【题目】“瓦罐浸来蟾有影,金刀剖破玉无瑕”。豆腐是营养丰富、历史悠久的中国美食。
(1)制作豆腐过程的流程如下:
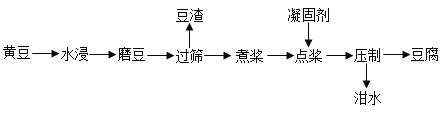

①豆腐制作过程中,利用过滤原理的是_________;(选填以上一种操作)
②“煮浆”时常用废木材作燃料,通常将废木材加工成废木屑,其原因是_________;
③“点浆”即在豆浆中加入某种盐,使溶解在水中的蛋白质溶解度变小而析出。加入的盐可能是___(填字母序号);
a BaCl2 b CuSO4 c MgCl2
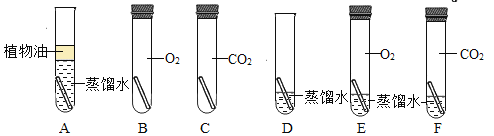
④下列扬州美食中,蛋白质含量最丰富的是____(填字母序号);

⑤豆腐与菠菜一般不能同食,因为豆腐中含有一种钙盐(CaSO4),菠菜中含有草酸(H2C2O4),两者会反应,生成草酸钙沉淀(CaC2O4),该反应的方程式为_______________。
(2)豆腐中含有人们生活所需的各类营养素,每100克豆腐中含各种营养成分如下表:
成分 | X | 蛋白质 | 油脂 | 糖类 | 钙 | 磷 | 铁 | 维生素B1 | 维生素B2 |
质量分数/% | 89.3 | 4.7 | 1.3 | 2.8 | 0.24 | 0.064 | 1.4 | 0.00006 | 0.00003 |
①表中X代表六大营养素中的_________________;
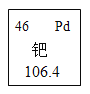
②摄入______________(填元素符号,下同)元素不足,易得佝偻病。钙、磷、铁元素中属于人体必需微量元素的是________________;
③蛋白质、油脂和葡萄糖中属于高分子化合物的是__________;
④某成年人若食用了500g豆腐,相当于补充了___________mg的维生素B1。
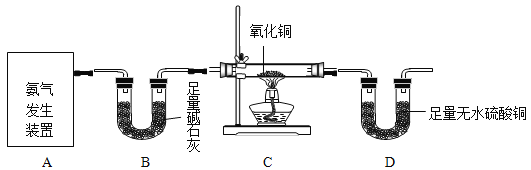
【题目】某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,流程如下:
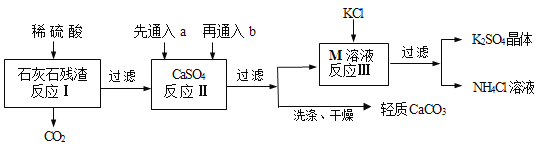
已知:CaCO3+H2O+CO2=Ca(HCO3)2
(1)为了提高反应Ⅰ的速率,下列措施中可行的是____________(填序号);
①搅拌
②将残渣粉碎成细小颗粒
③适当增大硫酸的浓度
(2)反应Ⅱ中a和b分别是_______________(填序号);
①足量CO2、适量NH3 ②足量NH3、适量CO2
③适量CO2、足量NH3 ④适量NH3、足量CO2
(3)反应Ⅲ中相关物质的溶解度如下表,该表中M物质的化学式为___________,反应Ⅲ在常温下能实现的原因是________,生成的NH4Cl溶液在农业上可用作_______________;
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)判断CaCO3固体已洗涤干净的方法:取最后一次洗涤液,______(①滴加稀盐酸、② 滴加Na2SO4 溶液、③ 滴加BaCl2溶液,填写序号),若无明显的现象,则已洗净;
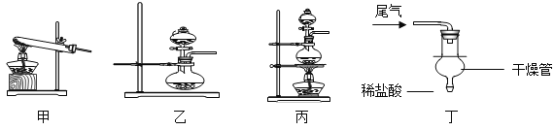
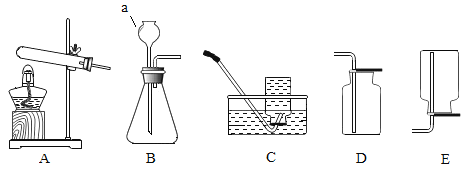
(5)过滤器的制作如图,正确的顺序是______(填序号);
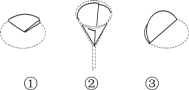
(6)该工艺流程中循环利用的物质除了水,还有_________________________。
【题目】某化学兴趣小组提出可以用废锌渣(主要成分是ZnO、FeO、Fe2O3、CuO)进行适当处理可制得硫酸锌晶体(ZnSO4·x H2O)。
Ⅰ、硫酸锌晶体的制备
该兴趣小组同学设计了如下流程:

已知:①硫酸锌晶体难溶于酒精
②硫酸锌晶体受热易逐步失去结晶水
③几种物质沉淀时的pH如下表:
物质 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
开始沉淀时pH | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 3.2 | 8.0 | 6.4 |
(1)酸浸中生成硫酸锌的化学方程式为___________,属于________(填基本类型)反应。
(2)酸浸时温度和时间对锌浸出率的影响见下图。为了提高锌的浸出率,反应的最佳温度是__________℃,最佳时间是____________min;
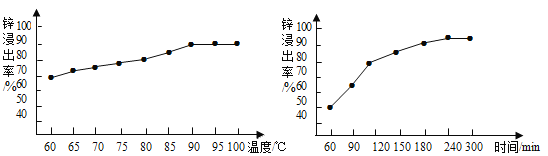
(3)加H2O2的目的是将酸浸后的Fe2+氧化成Fe3+,其反应方程式为2FeSO4 + H2O2 + _____= Fe2(SO4)3 + 2H2O,KMnO4溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,选择H2O2的优点是_________;
(4)加入ZnO调节溶液的pH约为4的目的是__________;
(5)流程中,滤渣Y的成分为_________________;
(6)流程中“一系列操作”主要过程为:①_________________ 、冷却结晶、过滤,加入酒精洗涤,重复几次,最后低温烘干,得到ZnSO4·xH2O;
②用酒精洗涤的目的是洗去晶体表面的杂质、避免因水洗涤所造成的晶体损耗、_________;
③低温烘干的原因是_______________。
Ⅱ、硫酸锌晶体(ZnSO4·xH2O)组成的测定
学习小组取5.74g硫酸锌晶体(ZnSO4·xH2O)进行加热分解,获得相关数据,并绘制成剩余固体质量一温度的关系图。
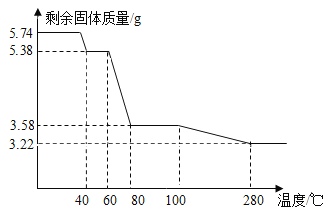
(7)280℃时,固体完全失去结晶水。根据图中数据,计算ZnSO4·xH2O中x的值为_____________;(请写出计算过程)
(8)加热过程中,硫酸锌晶体分步失去结晶水。请写出60℃到80℃时反应方程式_________。