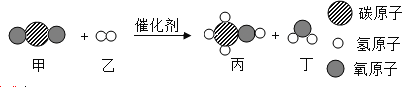
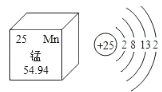
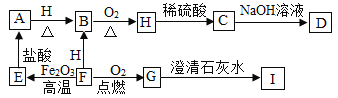
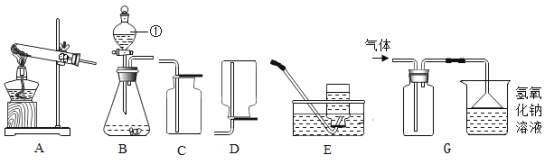
【题目】NaCl是重要的工业原料,工业上可用电解饱和食盐水的方法获取烧碱、氯气、氢气等物质。实验小组的同学现欲对一份久置的工业烧碱的成分进行探究。
(查阅资料)电解饱和食盐水的化学方程式为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(提出问题)小组同学根据相关信息,对工业烧碱的成分作了如下猜想:
猜想一:NaOH、NaCl
猜想二:Na2CO3、NaCl
猜想三:_________________;
(实验探究)
为了验证猜想,小组同学进行了实验探究。首先取工业烧碱样品少许,配成溶液,待用。
(1)取样品溶液少许,滴加足量稀盐酸,有气泡产生,说明样品中含有________(填化学式),写出产生气泡的化学反应的方程式_________________;工业烧碱中含有该物质的原因是________(用化学方程式表示)。
(2)为了证明样品中含有NaCl,小组同学设计实验方案如下:先取样品溶液少量,向其中滴加足量的稀盐酸至不再产生气泡时,再向溶液中滴加AgNO3溶液,出现白色沉淀,加入稀硝酸后,沉淀不溶解,则样品中一定含有氯化钠。老师指出上述方案不合理,请说明理由_____;
(3)小组同学为进一步确认样品是否还含有氢氯化钠,设计了如下实验方案,请你将其补充完整。
实验操作步骤 | 实验现象 | 实验结论 |
①取样品溶液少许,加入足量氯化钙溶液,充分反应后静置 ②取反应后的溶液适量,滴加无色酚酞试液 | ①___________ ②____________ | 该样品中一定含有NaOH |
(反思与评价)
经过研究,小组同学认为,上述方案中,除了使用氯化钙以外,利用下列物质也可得到同样的效果,你认为下列哪些试剂是可行的_________(填序号)。
A Ca(OH)2 B Ca(NO3)2 C Ba(NO3)2 D Ba(OH)2
(数据处理)
最终实验证实,该久置工业烧碱样品中含有氢氧化钠、氯化钠和碳酸钠。为了进一步确定该混合物中Na2CO3的质量分数,实验小组的同学取了10克该工业烧碱样品,加入足量的溶质质量分数为7.3%稀盐酸,实验测得生成CO2气体的质量与所加盐酸质量关系如图所示,请据图计算:
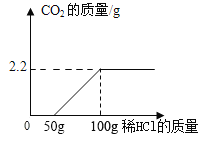
(1)该样品与稀盐酸完全反应时产生CO2的质量是____g。
(2)该样品中Na2CO3的质量分数____。