��Ŀ����
����Ŀ��ij��ȤС���ͬѧΪ�˲ⶨ̼������Ʒ��ֻ�����Ȼ��ƣ������������ʣ���̼���Ƶĺ�����ȡ�û������Ʒ������ϡ����ǡ����ȫ��Ӧ���й�ʵ�����ݼ�������
������ʵ������
��Ӧǰ | ��Ӧ�� | |||
ʵ������ | �ձ�������/g | ϡ���������/g | �������Ʒ������/g | �ձ������л���������/g |
40.6 | 123.4 | 12 | 171.6 | |
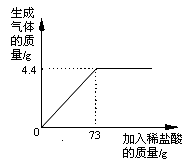
��1����Ӧ���ɶ�����̼������Ϊ g��
��2����Ʒ̼���Ƶ����������Ƕ��٣��������������0.1%��
��3����Ӧ��������Һ���������������Ƕ��٣�
���𰸡� ��1��4.4g;(2)88%;(3)10%
��������
�����������1�����ݻ�ѧ����ʽNa2CO3+2HCl�T2NaCl+H2O+CO2�����������غ㶨�ɿ�֪��Ӧǰ����ٵ������������ɶ�����̼����������40.6g+123.4g+12g��171.6g=4.4g��
��2������Ʒ��̼���Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 117 44
x y 4.4g
![]()
![]()
x=10.6g�� y=11.7g��
��Ʒ̼���Ƶ����������ǣ�![]() =88%��
=88%��
��3����Ӧ��������Һ���������������ǣ�![]() =10%��
=10%��
�𣺣�1����Ӧ���ɶ�����̼������Ϊ4.4g��
��2����Ʒ̼���Ƶ�����������88%��
��3����Ӧ��������Һ����������������10%��