题目内容
【题目】实验是科学探究的重要途径。以下是化学实验室中几种常用的实验装置,请回答有关问题:
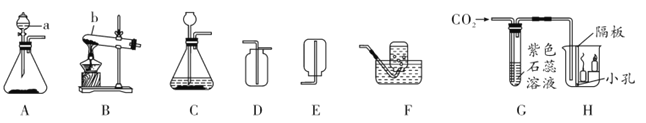
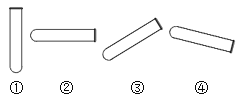
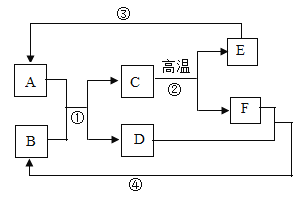
(1)写出图中标号仪器的名称:a___________________________,b___________________________。
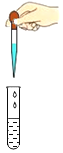
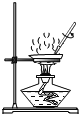
(2)实验室加热氯酸钾和二氧化锰制取氧气应选择的发生装置是___________________(填序号,下同),反应的化学方程式为___________________,想要收集比较纯净的氧气,应选择的装置是___________________。
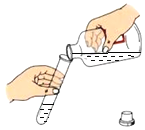
(3)实验室欲制取二氧化碳,选用A装置相对于C装置的优点是___________________,应选择的收集装置是___________________,反应的化学方程式为___________________,实验室检验CO2的方法是____________________________________________。
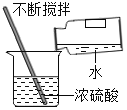
(4)将CO2通入紫色石蕊溶液,石蕊溶液变红,说明_________________________。烧杯H中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的化学性质是_________________________。
【答案】分液漏斗 试管 B  F 能够控制反应速率 D
F 能够控制反应速率 D ![]() 将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,说明该气体为CO2 二氧化碳 与水反应生成了酸性物质(或二氧化碳与水反应生成碳酸) 不燃烧也不支持燃烧
将产生的气体通入澄清石灰水中,若澄清石灰水变浑浊,说明该气体为CO2 二氧化碳 与水反应生成了酸性物质(或二氧化碳与水反应生成碳酸) 不燃烧也不支持燃烧
【解析】
(1)A为分液漏斗,b为试管;
(2)氯酸钾和二氧化锰加热制取氧气,是利用固体和固体加热制取气体,应该选择B装置,反应的化学方程式为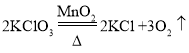 ;想要收集比较纯净的氧气,应选择排水法F。
;想要收集比较纯净的氧气,应选择排水法F。
(3)制取二氧化碳用石灰石与稀盐酸反应,是利用固体和液体不加热制取气体,选择A或C装置,A装置相对于C装置的优点是能够控制反应速率,反应的化学方程式为![]() ,二氧化碳密度比空气大,应选择向上排空气法收集。
,二氧化碳密度比空气大,应选择向上排空气法收集。
(4)由紫色石蕊溶液变红可知有酸性物质生成,即二氧化碳与水发生了反应,生成了碳酸;观察到烧杯中蜡烛由低到高依次熄灭,说明二氧化碳的物理性质为密度比空气大,化学性质为不燃烧也不支持燃烧。

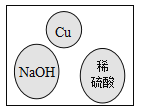
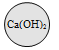
【题目】甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如图所示的四组实验方案。

(1)其中能达到实验目的的是_____。
(2)在C组实验中发生的化学方程式为_____。
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有_____生成(填化学式),滴入酚酞后溶液呈红色。
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性。使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和NaOH三种物质中的一种,或是三种物质两两混合组成的混合物。
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证。请根据要求完成下列空白:
实验内容 | 预测现象 | 结论 |
取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
③若有白色沉淀,溶液呈红色 | ___________________ |
(6)乙同学认为甲同学第②步验证的结论不严密,原因是_____。