题目内容
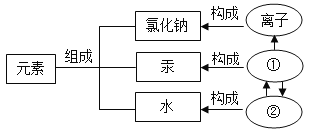
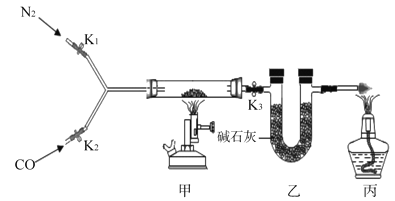
【题目】如图中的A~G表示几种初中化学常见的物质,其中A、B是单质,其他均是氧化物: C为红色粉末,B、E为黑色粉末;F是常温下无色液体。图中“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件己略去。
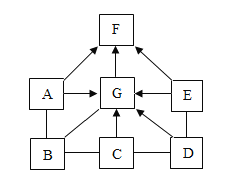
(1)写出F的化学式________;
(2)若E—D反应中有红色固体生成,则该反应方程式为:________;
(3)写出B—G反应的化学方程式为________;该反应的基本反应类型属于_______。
【答案】H2O CO+CuO![]() Cu+CO2 C+CO2
Cu+CO2 C+CO2![]() 2CO 化合反应
2CO 化合反应
【解析】
A、B是单质,其他均是氧化物,C为红色粉末氧化物,则C可能是氧化铁,E为黑色粉末氧化物,则E为可能氧化铜;F是常温下无色液体,则F可能是水;B为黑色固体单质,则B可能是碳;单质A能与碳反应,则A为氧气;G为气体二氧化碳;D是氧化物且能与氧化铜和氧化铁都能反应,则D是一氧化碳,代入框图进行验证,猜想成立。
(1)F是水,化学式为:H2O;
(2)若E—D反应中有红色固体生成,一氧化碳加热条件下与氧化铜反应产生铜和二氧化碳的反应方程式为:CO+CuO![]() Cu+CO2
Cu+CO2
(3)B—G:碳在高温条件下与二氧化碳反应产生一氧化碳的化学方程式为:C+CO2![]() 2CO;该反应符合“多变一”属于化合反应。
2CO;该反应符合“多变一”属于化合反应。

 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】某兴趣小组的同学对过氧化氢溶液制取氧气的实验进行如下探究。
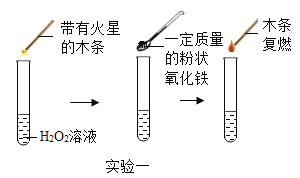
实验一:探究氧化铁能否作为过氧化氯分解的催化剂(实验过程如图所示)。
(1)图中实验能否证明氧化铁是过氧化氢分解的催化剂?并说明理由:____________。
(2)请写出过氧化氢溶液用二氧化锰作催化剂制取氧气的文字表达式:____________。
实验二:探究过氧化氢分解快慢的影响因素,实验过程如下表所示,
实验编号 | 过氧化氢溶液浓度 | 过氧化氢溶液质量 | 温度 | 二氧化锰粉末用量 | 氧气体积 | 反应所需时间 |
① | 5% | 12g | 20℃ | 0.2g | 125ml | 20s |
② | 30% | 12g | 20℃ | 0.2g | 125ml | 2s |
③ | 30% | 12g | 40℃ | 无 | 125ml | 148s |
(3)实验①和实验②中的变量是__________,得出的结论是____________。
(4)小明对比实验②和实验③得出结论:温度越高,过氧化氯分解速率越慢。你认为该结论是否可靠?___________(填“是”或“否”),理由是________________。
实验三:探究带火星的木条在不同体积分数的氧气中的复燃情况,部分实验数据记录如下表所示:
氧气体积分数(%) | 30 | 40 | 60 | 70 |
带火星的木条 | 不变 | 稍亮 | 复燃 | 复燃 |
(5)根据上述实验数据得出的结论是__________。在集气瓶中注入占其容积50%的水,用排水法收集氧气,将瓶内的水排尽,并用带火星的木条在该集气瓶中进行实验。推测实验现象,并说明理由:______。