题目内容
某校研究性学习小组的同学们,在进行课外社会调查实践活动中,发现一乡镇化工厂排出的废水部分流人了周边农田,导致庄稼长势迟缓甚至枯萎.同学们请教化学老师后知道废水中含有大量的FeSO4和CuSO4,工业废水的任意排放,不仅引起水体污染,使生态环境遭到破坏,还会浪费资源.于是同学们运用化学知识,对废水的处理设计了如下方案:
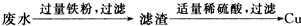
化工厂采纳了同学们的建议,解除了污染,也回收了铜.请你参与活动并回答下列问题:
(1)在此方案中,稀硫酸的作用是______,反应的化学方程式是______;
(2)回收铜的化学方程式是______,其反应类型是______.
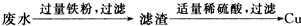
化工厂采纳了同学们的建议,解除了污染,也回收了铜.请你参与活动并回答下列问题:
(1)在此方案中,稀硫酸的作用是______,反应的化学方程式是______;
(2)回收铜的化学方程式是______,其反应类型是______.
(1)在此方案中,稀硫酸的作用是除去过量的铁粉,铁和稀硫酸反应能生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故填:除去过量的铁粉;Fe+H2SO4═FeSO4+H2↑.
(2)铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4,反应物和生成物都是一种单质和一种化合物,属于置换反应.
故填:Fe+CuSO4═Cu+FeSO4;置换反应.
故填:除去过量的铁粉;Fe+H2SO4═FeSO4+H2↑.
(2)铁比铜活泼,能和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4,反应物和生成物都是一种单质和一种化合物,属于置换反应.
故填:Fe+CuSO4═Cu+FeSO4;置换反应.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目


