题目内容
(2005?昆明)碳酸氢铵,俗称“碳铵”(化学式为NH4HCO3)是农村常用的氮肥.NH4HCO3受热容易分解,生成两种氧化物和氨气(化学式NH3).请你根据所学知识设计实验,证明下表中对两种氧化物的猜想:
写出“碳铵”受热分解的化学方程式
| 猜想 | 实验操作 | 实验现象 | 结论 |
| 一种是水蒸气 | 取适量NH4HCO3放在干燥试管中,并加热分解,再用无水硫酸铜检验生成的液滴. | ||
| 一种是二氧化碳 | 若出现浑浊 |
NH4HCO3
NH3↑+H2O+CO2↑
| ||
NH4HCO3
NH3↑+H2O+CO2↑
.根据NH4HCO3的这一性质,你认为“碳铵”这种化肥应如何保存
| ||
密封,放置在阴凉处
密封,放置在阴凉处
.分析:根据碳酸氢铵分解结合质量守恒定律,可猜想碳酸氢铵分解除生成氨气外,还可以生成二氧化碳和水;
白色无水硫酸铜粉末遇水变成蓝色,通常用来检验水的存在,因此,可选用该白色粉末检验碳酸铵受热分解的生成物中是否含水;二氧化碳能使澄清石灰水变浑浊,通过采用此方法检验气体为二氧化碳,因此,可采取把碳酸氢铵受热分解后的混合气体通入澄清石灰水检验是否含有二氧化碳.
根据质量守恒定律书写化学方程式,根据物质性质选择贮存方法和注意事项.
白色无水硫酸铜粉末遇水变成蓝色,通常用来检验水的存在,因此,可选用该白色粉末检验碳酸铵受热分解的生成物中是否含水;二氧化碳能使澄清石灰水变浑浊,通过采用此方法检验气体为二氧化碳,因此,可采取把碳酸氢铵受热分解后的混合气体通入澄清石灰水检验是否含有二氧化碳.
根据质量守恒定律书写化学方程式,根据物质性质选择贮存方法和注意事项.
解答:解:根据质量守恒定律,猜想碳酸氢铵受热分解除生成氨气外,还可以产生二氧化碳和水两种化合物;
为验证猜想,可把分解反产生的混合气体首先通过白色的无水硫酸铜粉末,若粉末变成蓝色,则可说明生成了水;再把混合气体通入澄清石灰水,若石灰水变浑浊,则可说明生成了二氧化碳;
故答案为:
“碳铵”受热分解的化学方程式为:NH4HCO3
NH3↑+H2O+CO2↑
因碳酸氢铵受热易分解,故应密封,放置在阴凉处.
为验证猜想,可把分解反产生的混合气体首先通过白色的无水硫酸铜粉末,若粉末变成蓝色,则可说明生成了水;再把混合气体通入澄清石灰水,若石灰水变浑浊,则可说明生成了二氧化碳;
故答案为:
| 猜想 | 实验操作 | 实验现象 | 结论 |
| 水蒸气 | 无水硫酸铜变成蓝色 | 碳酸氢铵受热分解的产物中有水 | |
| 二氧化碳 | 再把混合气体通过澄清的石灰水 | 碳酸氢铵受热分解的产物中有二氧化碳 |
| ||
因碳酸氢铵受热易分解,故应密封,放置在阴凉处.
点评:根据反应的描述猜测生成物时,要遵循质量守恒定律,根据反应前后元素种类不变的原则对生成物进行合理猜想;违背质量守恒定律的猜想都是不正确的猜想,也就无探究的价值和必要.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
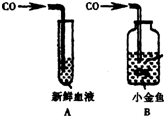 (2005?昆明)(1)写出工业上高温煅烧石灰石的化学反应方程式
(2005?昆明)(1)写出工业上高温煅烧石灰石的化学反应方程式