题目内容
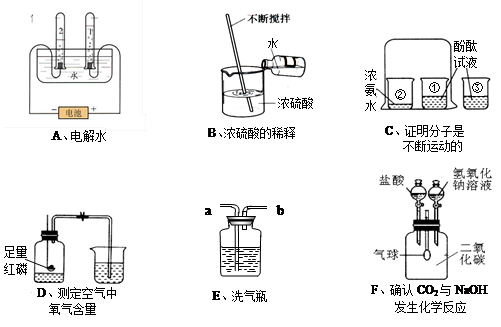
(6分)(2012?昭通)根据如图所示的实验A、B、C,回答问题(1)~(3).
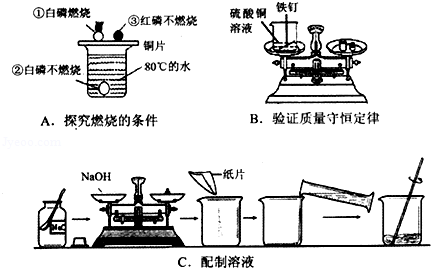
(1)实验A中,铜片上的红磷没有燃烧,说明燃烧需要 _________ .
(2)实验B中,能充分证明质量守恒定律的现象是 _________ ,从微观角度分析质量守恒的原因是 _________ .
(3)实验C中的一处明显错误是 _________ ,如果量取水时,仰视读数,配得的氢氧化钠溶液中溶质的质量分数将 _________ (填“偏大”、“偏小”或“不变”),配置好的氢氧化钠溶液必须密封保存,原因是 _________ .

(1)实验A中,铜片上的红磷没有燃烧,说明燃烧需要 _________ .
(2)实验B中,能充分证明质量守恒定律的现象是 _________ ,从微观角度分析质量守恒的原因是 _________ .
(3)实验C中的一处明显错误是 _________ ,如果量取水时,仰视读数,配得的氢氧化钠溶液中溶质的质量分数将 _________ (填“偏大”、“偏小”或“不变”),配置好的氢氧化钠溶液必须密封保存,原因是 _________ .
(1)达到着火点.
(2)天平仍保持平衡;反应前后的原子个数,质量分数,种类不变.
(3)偏小;氢氧化钠接触空气中的二氧化碳而变质.
(2)天平仍保持平衡;反应前后的原子个数,质量分数,种类不变.
(3)偏小;氢氧化钠接触空气中的二氧化碳而变质.
(1)根据燃烧的条件可知,铜片上的红磷与空气接触,是可燃物,但不能燃烧,说明是没有达到着火点,说明燃烧需要达到着火点.
故答案为:达到着火点.
(2)硫酸铜溶液能与铁钉反应,但天平仍然能够保持平行,可以证明质量守恒定律现象;从微观角度分析质量守恒的原因是:反应前后的原子个数,质量分数,种类不变.
故答案为:天平仍保持平衡;反应前后的原子个数,质量分数,种类不变.
(3)若其它操作都正确,而只有在量取水时仰视读数,仰视时所读取的数据小于所量水的实际体积,即量取水的体积大于实际所需水的量.由于溶剂水的质量偏大,根据溶液的溶质质量分数= ×100%,可判断如此操作所配溶液溶质的质量分数比实际的偏小;氢氧化钠溶液需要密封保存是因为它接触空气中的二氧化碳而变质
×100%,可判断如此操作所配溶液溶质的质量分数比实际的偏小;氢氧化钠溶液需要密封保存是因为它接触空气中的二氧化碳而变质
故答案为:偏小;氢氧化钠接触空气中的二氧化碳而变质.
故答案为:达到着火点.
(2)硫酸铜溶液能与铁钉反应,但天平仍然能够保持平行,可以证明质量守恒定律现象;从微观角度分析质量守恒的原因是:反应前后的原子个数,质量分数,种类不变.
故答案为:天平仍保持平衡;反应前后的原子个数,质量分数,种类不变.
(3)若其它操作都正确,而只有在量取水时仰视读数,仰视时所读取的数据小于所量水的实际体积,即量取水的体积大于实际所需水的量.由于溶剂水的质量偏大,根据溶液的溶质质量分数=
 ×100%,可判断如此操作所配溶液溶质的质量分数比实际的偏小;氢氧化钠溶液需要密封保存是因为它接触空气中的二氧化碳而变质
×100%,可判断如此操作所配溶液溶质的质量分数比实际的偏小;氢氧化钠溶液需要密封保存是因为它接触空气中的二氧化碳而变质故答案为:偏小;氢氧化钠接触空气中的二氧化碳而变质.

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案
相关题目