题目内容
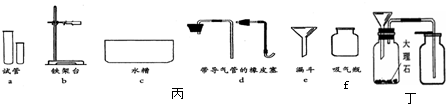
某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究.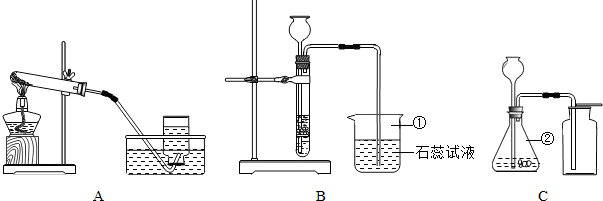
(1)写出下列编号仪器的名称:①
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的
该反应的化学方程式是
(3)下列化学变化中,氧气不作为反应物的是
①天然气燃烧 ②缓慢氧化 ③光合作用 ④钢铁生锈
(4)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释是
A.产生的CO2直接使石蕊试液变红式
B.产生的CO2与水反应生成H2CO3使石蕊试液变红
C.挥发出的氯化氢溶于水使石蕊试液变红
(5)丙同学用C装置制取了一瓶无色无味的气体(纯净物),你推测该气体可能是
分析:(1)①②均为实验室常用的仪器.
(2)根据反应物的状态和反应条件确定发生装置;熟记常用的化学方程式;实验结束时若先熄灭酒精灯,装置内的温度降低,气体收缩,气体压强减小,在外界大气压的作用下水槽中的水被压入试管,热的试管遇冷炸裂.
(3)①要消耗氧气;②要消耗氧气;③有氧气生成;④要消耗氧气.
(4)根据二氧化碳的化学性质和盐酸的挥发性进行分析.
(5)使用该装置必须满足的条件是:反应物的状态是固态和液态,反应条件是常温,生成气体的密度比空气大;根据所制取气体的性质进行检验.
(2)根据反应物的状态和反应条件确定发生装置;熟记常用的化学方程式;实验结束时若先熄灭酒精灯,装置内的温度降低,气体收缩,气体压强减小,在外界大气压的作用下水槽中的水被压入试管,热的试管遇冷炸裂.
(3)①要消耗氧气;②要消耗氧气;③有氧气生成;④要消耗氧气.
(4)根据二氧化碳的化学性质和盐酸的挥发性进行分析.
(5)使用该装置必须满足的条件是:反应物的状态是固态和液态,反应条件是常温,生成气体的密度比空气大;根据所制取气体的性质进行检验.
解答:解:(1)熟记常用仪器的名称可知①为烧杯,②为锥形瓶.
(2)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;高锰酸钾加热生成锰酸钾、二氧化锰和氧气;实验结束时应先把导管移出水面后熄灭酒精灯,防止冷水倒流,试管炸裂;氧气约占空气体积的五分之一.故答案为:A 2KMnO4
K2MnO4+MnO2+O2↑ 把导管移出水面 熄灭酒精灯 1/5
(3)①②④的反应物中都有氧气,③是生成物中有氧气.故答案为:③
(4)二氧化碳并不能使紫色的石蕊溶液变红,是二氧化碳与水反应生成的碳酸使紫色的石蕊溶液变红;盐酸具有挥发性,从盐酸中挥发出的氯化氢气体极易溶于水,溶于水后又成了盐酸,盐酸能使紫色的石蕊溶液变红.故答案为:BC
(5)用稀盐酸与大理石反应制取二氧化碳可用此装置,二氧化碳能使澄清的石灰水变浑浊,可用澄清的石灰水检验是否是二氧化碳;用过氧化氢溶液与二氧化锰制氧气也可用此装置,氧气能使带火星的木条复燃,可用带火星的木条检验是否是氧气.故答案为:二氧化碳 在集气瓶内倒入少量澄清的石灰水,振荡,若澄清的石灰水变浑浊则说明是二氧化碳 (或氧气 把带火星的木条放入集气瓶中,若木条复燃,则说明是氧气.)
(2)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;高锰酸钾加热生成锰酸钾、二氧化锰和氧气;实验结束时应先把导管移出水面后熄灭酒精灯,防止冷水倒流,试管炸裂;氧气约占空气体积的五分之一.故答案为:A 2KMnO4
| ||
(3)①②④的反应物中都有氧气,③是生成物中有氧气.故答案为:③
(4)二氧化碳并不能使紫色的石蕊溶液变红,是二氧化碳与水反应生成的碳酸使紫色的石蕊溶液变红;盐酸具有挥发性,从盐酸中挥发出的氯化氢气体极易溶于水,溶于水后又成了盐酸,盐酸能使紫色的石蕊溶液变红.故答案为:BC
(5)用稀盐酸与大理石反应制取二氧化碳可用此装置,二氧化碳能使澄清的石灰水变浑浊,可用澄清的石灰水检验是否是二氧化碳;用过氧化氢溶液与二氧化锰制氧气也可用此装置,氧气能使带火星的木条复燃,可用带火星的木条检验是否是氧气.故答案为:二氧化碳 在集气瓶内倒入少量澄清的石灰水,振荡,若澄清的石灰水变浑浊则说明是二氧化碳 (或氧气 把带火星的木条放入集气瓶中,若木条复燃,则说明是氧气.)
点评:在实验室做实验时,一定要严格按照实验操作规则进行,否则,轻则会造成实验失败,重则会造成实验事故.

练习册系列答案
相关题目



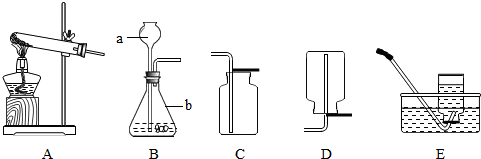
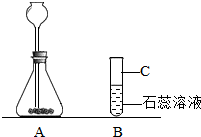
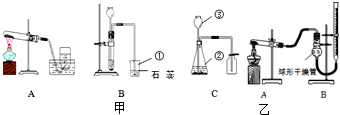
 (2007?莆田)某化学兴趣小组利用如图装置进行饱和NaCl溶液的电解实验,并对部分产物进行探究.
(2007?莆田)某化学兴趣小组利用如图装置进行饱和NaCl溶液的电解实验,并对部分产物进行探究.