题目内容
南京某中学学习小组考察过溶洞后,为溶洞中形态各异的石笋和钟乳石而惊叹,决定设计和实施简单的实验——模拟溶洞的“形成”。从教材上查得如下资料:
溶洞都分布在石灰岩组成的山地中,石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O==Ca(HCO3)2
溶有碳酸氢钙的水遇热或当压强突然变小时,溶解在水里的碳酸氢钙就会分解,重新生成碳酸钙沉积下来,同时放出二氧化碳: Ca(HCO3)2==CaCO3↓+CO2↑+H2O
洞顶的水在慢慢向下渗透时,水中的碳酸氢钙发生上述反应,有的沉积在洞顶,有的沉积在洞底,日积月累,洞顶的形成钟乳石,洞底的形成石笋,当钟乳石与石笋相连时就形成了石柱。
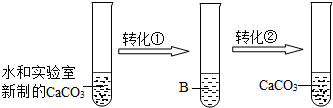
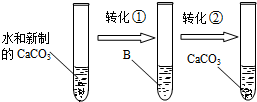
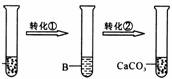
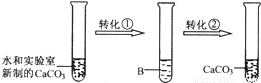
(1)他们设计并完成了模拟溶洞“形成”的实验。其实验过程如下图,试回答:
 实现转化①需要通入足量的气体A,A的化学式是__________;B溶液中溶质的化学式是__________;
实现转化①需要通入足量的气体A,A的化学式是__________;B溶液中溶质的化学式是__________;
实现转化②,通常采用的基本操作方法是__________。
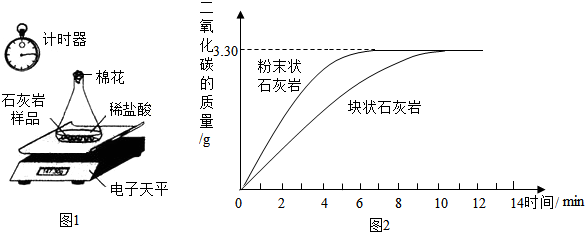
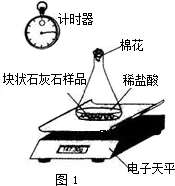
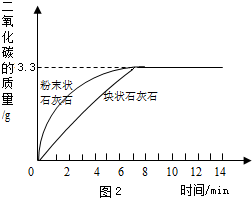
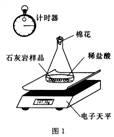
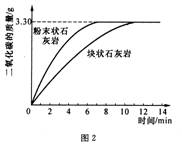
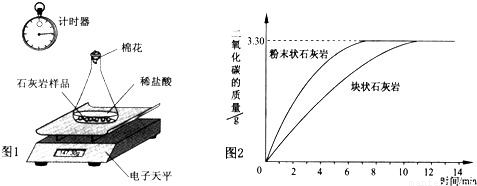
(2)他们用采集的石灰岩样品进行相关实验。将采集到的样品用水冲洗后晾干,称取24.00g样品平均分成两份,分别与足量相同质量分数的稀盐酸反应进行下列测定(如图1),经数据处理得到释放出二氧化碳的质量与反应时间的关系图(如图2)。
 |
①图1所示实验中数据记录纸上应该连续记录的实验数据是_________和_________。
②由图2中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越__________,其反应速率越__________。
③试求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
(1)CO2 Ca(HCO3)2 加热
(2)①电子天平示数(或锥形瓶体系质量) 计时器示数(或反应时间)(答案不分先后顺序)
②大 快 (或小 慢)
③解:设每份样品中CaCO3的质量为x
 CaCO3+2HCl==CaCl2+H2O+CO2↑
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
x 3.30g
24.00g÷2=12g 7.5g÷12g×100%=62.5% 答:样品中CaCO3质量分数为62.5%

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案