题目内容
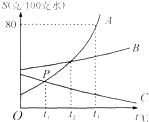 如图是A、B、C三种物质的溶解度曲线,根据图示信息,回答下列问题.
如图是A、B、C三种物质的溶解度曲线,根据图示信息,回答下列问题.(1)P点表示:
t1℃时,SA=SC
t1℃时,SA=SC
,t1℃~t2℃
t1℃~t2℃
时,SB>SA>SC(2)若在t3℃时,A的饱和溶液中含有少量的B,把A、B二种物质进行分离的方法可用
冷却热饱和溶液
冷却热饱和溶液
.C
C
(A、B、C)溶液由饱和转化为不饱和,可采用降温的方法.(3)
t2
t2
℃时,A、B饱和溶液的溶质质量分数相等.(4)t3℃时,把50克A与60克水混合,
能
能
(能或不能)配成该温度下的饱和溶液,溶液的质量是108
108
克,溶液的溶质质量分数是44.4%
44.4%
.分析:(1)根据两条溶解度曲线的交点说明此温度下两种物质的溶解度相等,同一温度下溶解度曲线越高的溶解度越大解答;
(2)根据溶解度受温度影响大的溶解度受温度影响小的固体可以用冷却热饱和溶液的方法分离,根据溶解度曲线的走向判断固体物质溶解度受温度的影响情况解答;
(3)根据两条溶解度曲线的交点说明此温度下两种物质的溶解度相等,饱和溶液溶质质量分数=
×100%解答;
(4)根据t3℃时A的溶解度是80g分析计算.
(2)根据溶解度受温度影响大的溶解度受温度影响小的固体可以用冷却热饱和溶液的方法分离,根据溶解度曲线的走向判断固体物质溶解度受温度的影响情况解答;
(3)根据两条溶解度曲线的交点说明此温度下两种物质的溶解度相等,饱和溶液溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
(4)根据t3℃时A的溶解度是80g分析计算.
解答:解:(1)点P是A、C溶解度曲线的交点,说明此时二者的溶解度相等;温度高于t1℃,低于t2℃时SB>SA>SC;
故答案:t1℃时,SA=SC;t1℃~t2℃.
(2)A的溶解度受温度影响较大且随温度升高而增大,B的溶解度受温度影响较小,所以降低温度,A会大量的结晶析出,B几乎不会析出晶体;C的溶解度随温度的降低而增大,饱和溶液会变成不饱和溶液,
故答案:冷却热饱和溶液;C.
(3)t2℃A和B的溶解度相等,又饱和溶液溶质质量分数=
×100%,所以此时A、B饱和溶液的溶质质量分数相等.
故答案:t2
(4)t3℃时A的溶解度是80g,此温度下100g水中最多溶解80gA,所以此温度下60g水中最多溶解48gA,剩余2gA,饱和溶液质量为48g+60g=108g,溶液中溶质质量分数为=
×100%=44.4%,
故答案:能;108g;44.4%.
故答案:t1℃时,SA=SC;t1℃~t2℃.
(2)A的溶解度受温度影响较大且随温度升高而增大,B的溶解度受温度影响较小,所以降低温度,A会大量的结晶析出,B几乎不会析出晶体;C的溶解度随温度的降低而增大,饱和溶液会变成不饱和溶液,
故答案:冷却热饱和溶液;C.
(3)t2℃A和B的溶解度相等,又饱和溶液溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
故答案:t2
(4)t3℃时A的溶解度是80g,此温度下100g水中最多溶解80gA,所以此温度下60g水中最多溶解48gA,剩余2gA,饱和溶液质量为48g+60g=108g,溶液中溶质质量分数为=
| 48g |
| 108g |
故答案:能;108g;44.4%.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
 17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.
17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题. 29、如图是a、b、c三种固体物质的溶解度曲线图.
29、如图是a、b、c三种固体物质的溶解度曲线图. 16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答: (1)如图是A、B、C三种物质的溶解度曲线.请回答:
(1)如图是A、B、C三种物质的溶解度曲线.请回答:
