题目内容
某学生为了分析Na2S04样品是否含有NaCl,他设计了如下列实验:
①取固体溶于水,配制成溶液。
②在上述溶液中,加入过量的试剂A,生成白色沉淀,过滤。
③在②的滤液中加入过量的Na2S03溶液中,生成白色沉淀,过滤。
④在③的滤液中加入过量的试剂B,有气体放出。
⑤在④溶液中滴入AgN03溶液,有白色沉淀生成,由此他得山结论:有NaCl存在。
请你分析写出:试剂的化学式 ,试剂B的化学式 ;步骤②的作用是 :步骤⑧的作用是 ;步骤④的作用是 。
Ba(N03)2稀硝酸 完全除去SO2- 4,除掉②中的加入的过量的Ba2+。完全除掉CO2- 3。

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目

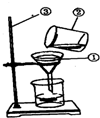 某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置进行过滤.
某学生为了使一杯浑浊的食盐水变成澄清透明,利用了如图所示的装置进行过滤.