题目内容
【题目】如图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属。
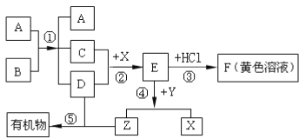
请回答下列问题:
(1)写出C物质的化学式:___________;
(2)反应①中A物质的作用是___________;
(3)反应③、④的化学方程式:③___________;④_____________;
(4)在日常生活中为防止反应②的发生,可采取的措施是_______(写一点即可);
(5)在自然界中普遍存在反应⑤,其名称为__________。
【答案】O2 催化作用 Fe2O3+6HCl=2FeCl3+3H2O Fe2O3 +3CO![]() 2Fe+3CO2 刷漆 光合作用
2Fe+3CO2 刷漆 光合作用
【解析】
同种元素组成的无色液体有过氧化氢和水,过氧化氢具有消毒杀菌作用, B是过氧化氢,D是水,实验室常用二氧化锰催化过氧化氢制取氧气,且A为黑色固体粉末,可知A是二氧化锰, C就是氧气,最常见的金属是铁,铁和氧气、水蒸气反应生成铁锈,又因为E和盐酸反应后得到黄色溶液,可以确定X是铁,E是铁锈且符合“E为固体氧化物”的条件,铁锈能和有毒的无色气体 Y反应生成铁和Z,Y是一氧化碳,Z是二氧化碳,二氧化碳和水在叶绿素和光合作用下反应生成葡萄糖和氧气,葡萄糖是有机物,符合题意;
(1)C是氧气,故填O2;
(2)物质A是二氧化锰,反应①是二氧化锰催化过氧化氢的反应,二氧化锰做催化剂,故填催化作用;
(3)E是氧化铁,Y是一氧化碳,③是氧化铁和盐酸反应生成氯化铁和水的反应,故填Fe2O3+6HCl=2FeCl3+3H2O;④是一氧化碳还原氧化铁生成二氧化碳和铁的反应,故填Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(4)反应②是铁和氧气水蒸气发生的铁的锈蚀,保持铁质容器表面干燥、涂油、刷漆或者制成不锈钢都可以防锈,故填刷漆;
(5)反应⑤是二氧化碳和水在叶绿素和光合作用下反应生成葡萄糖和氧气,故填光合作用。

 阅读快车系列答案
阅读快车系列答案【题目】如下图(夹持仪器已略),某兴趣小组在老师指导下,探究铁与水蒸气的反应,请回答。
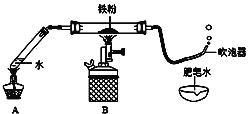
【实验初探】
(1)连接装置,并___________。
(2)装好药品。
(3)加热一段时间后,吹泡器连续吹出气泡,且气泡向上飞起,用燃着的木条靠近气泡,能产生爆鸣。
该气体燃烧的化学方程式为________。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4)。
①它们都不溶于水,其中铁粉、Fe3O4能被磁铁吸引;②FeO接触到空气会立即由黑色变为红棕色;③三种氧化物都不与硫酸铜溶液反应,但能与酸反应生成可溶性物质。
【实验探究】实验小组同学对反应后的剩余固体进行探究。
(1)小梅发现固体为黑色,由此判断:固体中肯定不存在Fe2O3 ,理由是_______。
(2)小宇发现固体均能被磁铁吸引,大家倒出玻璃管中黑色固体,平铺于白纸上。观察现象是__________,判断黑色固体中一定没有FeO。
讨论:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【提出猜想】玻璃管中黑色固体成分有什么?
猜想Ⅰ:Fe; 猜想Ⅱ:Fe3O4; 猜想Ⅲ:______________
实验步骤 | 实验现象 | 实验结论 |
取上述固体少许,加入足量 _________________ | 出现红色固体,且有黑色固体残留 | 黑色固体中一定含有 ________________ |
【结论反思】(1)铁与水蒸气发生置换反应,反应的方程式是________________。
(2)出现红色固体的化学方程式是_______,加入的溶液必须足量的原因是______________。
【题目】某化学学习兴趣小组为了测定某生理盐水的溶质质量分数,实验过程和有关实验数据如图所示:

根据上图信息解决下列问题:
(1)已知过滤后获得的固体物质是一种纯净物,则该物质的名称是____________,质量是__________g。
(2)该生理盐水的溶质质量分数是多少?(写出运算过程)________________
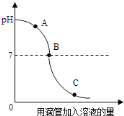
(3)请在图上作出往生理盐水滴加 AgNO3 溶液, 产生 AgCl 沉淀的质量与参与反应的 AgNO3 溶液的质量之间的关系图像。__________
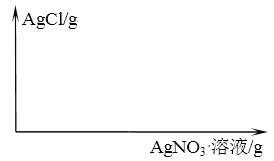
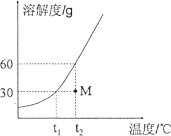
(4)已知硝酸钠的溶解度如表所示,据此估算判断该实验获得的 161.13g 溶液在常温下属于___________________溶液(填“饱和”或“不饱和”)。
硝酸钠在水中的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
溶解度/g | 73 | 80 | 87 | 98 | 103 | 113 | 124 | 137 | 150 | 163 | 180 |