题目内容
金属材料在生活、生产中应用十分广泛.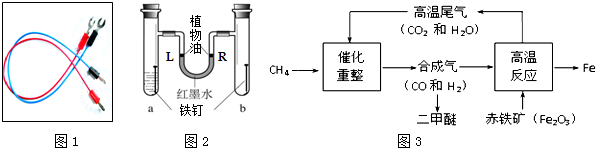
(1)图1是利用金属具有
(2)生活中使用的大多是合金而不是纯金属,这是因为合金具有更多优 良性能,例如钢的硬度比纯铁
(3)铁制品很易锈蚀,某同学设计了图2所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察现象.①此实验中蕴含的化学思想方法是
A.只有a管中的铁钉会锈蚀
B.L端与R端的液面高度仍然保持一致
C.该实验不能说明铁生锈与空气有关
D.该实验说明铁的锈蚀与空气和水有关
(4)若用“一种金属单质,两种盐溶液”验证锌、银、铜三种金属活动性顺序,则验证过程中所涉及的化学方程式为
(5)合成气(CO和H2)不仅用于制备被称为21世纪新型燃料的二甲醚(CH3OCH3),同时还用于冶炼金属,其部分生产过程示意图如图3:
①二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得.反应过程中CO和H2按分子个数比1:2进行反应,制得二甲醚时,生成的另一种物质是
②根据示意图中标示的物质,合成气在冶炼铁的生产过程中发生了两个重要的反应,其中不属于置换反应的化学方程式为

(1)图1是利用金属具有
导电性
导电性
性的实例.(2)生活中使用的大多是合金而不是纯金属,这是因为合金具有更多优 良性能,例如钢的硬度比纯铁
大
大
(填“大”或“小”).(3)铁制品很易锈蚀,某同学设计了图2所示的装置探究铁锈蚀的条件.a管中装入少量煮沸的蒸馏水,b管中是干燥的空气.调节L端与R端的液面高度一致,塞紧木塞.一段时间后观察现象.①此实验中蕴含的化学思想方法是
对比法
对比法
.②下列推断错误的是BC
BC
.A.只有a管中的铁钉会锈蚀
B.L端与R端的液面高度仍然保持一致
C.该实验不能说明铁生锈与空气有关
D.该实验说明铁的锈蚀与空气和水有关
(4)若用“一种金属单质,两种盐溶液”验证锌、银、铜三种金属活动性顺序,则验证过程中所涉及的化学方程式为
Cu+2AgNO3=Cu(NO3)2+2Ag
Cu+2AgNO3=Cu(NO3)2+2Ag
.用铝丝与硫酸铜溶液反应完成“铜树”实验时,先要除去铝丝表面的氧化膜,常用的物理方法是用砂纸打磨
用砂纸打磨
,若用稀盐酸处理,当看到有气泡产生
有气泡产生
时,表明氧化膜已被破坏.(5)合成气(CO和H2)不仅用于制备被称为21世纪新型燃料的二甲醚(CH3OCH3),同时还用于冶炼金属,其部分生产过程示意图如图3:
①二甲醚(CH3OCH3)可由合成气(CO和H2)在一定的条件下制得.反应过程中CO和H2按分子个数比1:2进行反应,制得二甲醚时,生成的另一种物质是
H2O
H2O
.②根据示意图中标示的物质,合成气在冶炼铁的生产过程中发生了两个重要的反应,其中不属于置换反应的化学方程式为
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
,检验高温尾气中含有二氧化碳的化学反应方程式为
| ||
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.分析:(1)铜做导线是利用铜的导电性
(2)根据合金的性质进行分析.
(3)铁在空气中生锈,主要是铁跟水和氧气等物质相互作用的结果,通过a、b两管中反应条件的比较a管中有水反应速度应快些,气压相对低了,红墨水的水平就变化了;
(4)只用一种金属单质,该金属就是排在中间的金属,根据铜与硝酸银反应的方程式进行书写即可;除去氧化膜一般用砂纸打磨;根据盐酸与铝反应的现象考虑;
(5)①根据反应前后各种原子个数和种类不变考虑;②根据置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物进行判断,并写出相应的化学方程式.
(2)根据合金的性质进行分析.
(3)铁在空气中生锈,主要是铁跟水和氧气等物质相互作用的结果,通过a、b两管中反应条件的比较a管中有水反应速度应快些,气压相对低了,红墨水的水平就变化了;
(4)只用一种金属单质,该金属就是排在中间的金属,根据铜与硝酸银反应的方程式进行书写即可;除去氧化膜一般用砂纸打磨;根据盐酸与铝反应的现象考虑;
(5)①根据反应前后各种原子个数和种类不变考虑;②根据置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物进行判断,并写出相应的化学方程式.
解答:解:(1)铜做导线是利用铜的导电性;
(2)合金的硬度比纯金属要大,钢就比纯铁硬度大的多,故答案为:大;
(3)A、只有a管中的铁钉会锈蚀.b管中是干燥的空气,铁在干燥的空气中很难生锈,故A正确;
B、铁在空气中生锈,主要是铁跟水和氧气等物质反应,a管中有水反应速度应快些,气压相对低了,红墨水的水平就升高了,故B错误;
C、该实验能够说明铁锈蚀与空气有关,故C错误;
D、该实验说明铁的锈蚀与空气和水有关 实验结果是L端红墨水上升了,说明a管中铁生锈快,证明铁的生锈与水和空气有关,故C正确. 故选BC.
(4)只用一种金属单质,该金属就是排在中间的金属,所以该金属是铜,铜与铝的盐溶液不反应,铜与硝酸银反应生成银和硝酸铜,用观察法配平即可,所以方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag;除去铝表面的氧化膜一般用砂纸打磨;铝把氧化膜反应完后,会与铝反应,铝与盐酸反应生成氯化铝和氢气,所以当有气泡冒出,说明已经把氧化膜反应完了;
(5)①二甲醚(CH3OCH3)的一个分子中含有2个C,6个H,1个O,因为CO和H2按分子个数比1:2,所以需要2个CO分子和4个H2分子,所以多出了2个H,1个O,所以生成物中还有水(或H2O);
②由于一氧化碳、氢气都具有还原性,都能与氧化铁反应,一氧化碳与氧化铁反应的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,不属于置换反应,反应条件是高温,用观察法配平即可;所以化学方程式是:3CO+Fe2O3
2Fe+3CO2.正确书写,检验高温尾气中含有二氧化碳的化学反应方程式为 CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:(1)导电性; (2)大; (3)①对比法; ②BC;
(4)Cu+2AgNO3=Cu(NO3)2+2Ag; 用砂纸打磨; 有气泡产生;
(5)①H2O; ②3CO+Fe2O3
2Fe+3CO2;CO2+Ca(OH)2=CaCO3↓+H2O
(2)合金的硬度比纯金属要大,钢就比纯铁硬度大的多,故答案为:大;
(3)A、只有a管中的铁钉会锈蚀.b管中是干燥的空气,铁在干燥的空气中很难生锈,故A正确;
B、铁在空气中生锈,主要是铁跟水和氧气等物质反应,a管中有水反应速度应快些,气压相对低了,红墨水的水平就升高了,故B错误;
C、该实验能够说明铁锈蚀与空气有关,故C错误;
D、该实验说明铁的锈蚀与空气和水有关 实验结果是L端红墨水上升了,说明a管中铁生锈快,证明铁的生锈与水和空气有关,故C正确. 故选BC.
(4)只用一种金属单质,该金属就是排在中间的金属,所以该金属是铜,铜与铝的盐溶液不反应,铜与硝酸银反应生成银和硝酸铜,用观察法配平即可,所以方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag;除去铝表面的氧化膜一般用砂纸打磨;铝把氧化膜反应完后,会与铝反应,铝与盐酸反应生成氯化铝和氢气,所以当有气泡冒出,说明已经把氧化膜反应完了;
(5)①二甲醚(CH3OCH3)的一个分子中含有2个C,6个H,1个O,因为CO和H2按分子个数比1:2,所以需要2个CO分子和4个H2分子,所以多出了2个H,1个O,所以生成物中还有水(或H2O);
②由于一氧化碳、氢气都具有还原性,都能与氧化铁反应,一氧化碳与氧化铁反应的反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,不属于置换反应,反应条件是高温,用观察法配平即可;所以化学方程式是:3CO+Fe2O3
| ||
故答案为:(1)导电性; (2)大; (3)①对比法; ②BC;
(4)Cu+2AgNO3=Cu(NO3)2+2Ag; 用砂纸打磨; 有气泡产生;
(5)①H2O; ②3CO+Fe2O3
| ||
点评:本题通过实验探究的方法考查了铁锈蚀的条件,培养了学生的实验探究能力;通过回答本题知道了金属的性质,保护金属资源的途径,方程式的书写方法.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目

 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.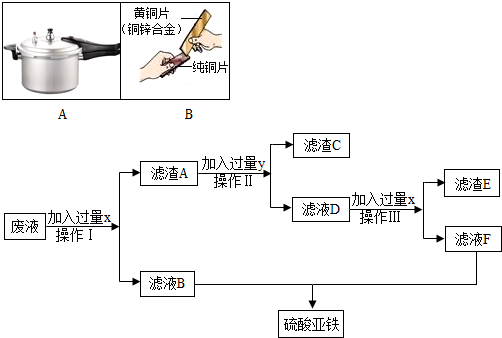
 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛. 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.