题目内容
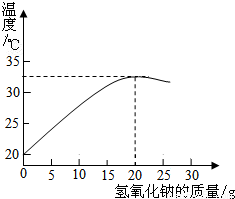
右图表示质量分数为8%的氢氧化钠溶液与20g某浓度稀盐酸发生反应后溶液温度的变化情况.
①根据曲线判断,当加入氢氧化钠溶液的质量为______时,反应恰好完全进行.
②当加入15g氢氧化钠溶液时,所得溶液中的溶质为______(写化学式).
③试计算该稀盐酸中溶质的质量分数(请写出计算过程).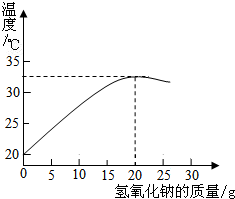
①根据曲线判断,当加入氢氧化钠溶液的质量为______时,反应恰好完全进行.
②当加入15g氢氧化钠溶液时,所得溶液中的溶质为______(写化学式).
③试计算该稀盐酸中溶质的质量分数(请写出计算过程).

①根据曲线可以看出,加入氢氧化钠溶液的质量为20g时二者恰好完全反应,所以本题答案为:20g;
②根据曲线可以看出,加入氢氧化钠溶液的质量为20g时二者恰好完全反应,而15g氢氧化钠溶液时有剩余的盐酸.故答案为HCl和NaCl;
③设稀盐酸中溶质质量为x
NaOH+HCl═NaCl+H2O
40 36.5
20×8% x
=
x=1.46g
盐酸的质量分数为
×100%=7.3%
答:稀盐酸的溶质质量分数为7.3%.
故本题的答案为:
①20g②NaCl和HCl③7.3%.
②根据曲线可以看出,加入氢氧化钠溶液的质量为20g时二者恰好完全反应,而15g氢氧化钠溶液时有剩余的盐酸.故答案为HCl和NaCl;
③设稀盐酸中溶质质量为x
NaOH+HCl═NaCl+H2O
40 36.5
20×8% x
| 40 |
| 20g×8% |
| 36.5 |
| x |
x=1.46g
盐酸的质量分数为
| 1.46g |
| 20g |
答:稀盐酸的溶质质量分数为7.3%.
故本题的答案为:
①20g②NaCl和HCl③7.3%.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
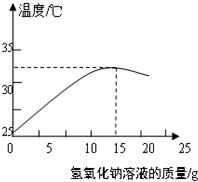 32、右图表示质量分数为8%的氢氧化钠溶液与20g某浓度稀盐酸发生反应后溶液温度的变化情况.
32、右图表示质量分数为8%的氢氧化钠溶液与20g某浓度稀盐酸发生反应后溶液温度的变化情况.
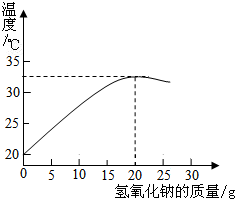 右图表示质量分数为8%的氢氧化钠溶液与20g某浓度稀盐酸发生反应后溶液温度的变化情况.
右图表示质量分数为8%的氢氧化钠溶液与20g某浓度稀盐酸发生反应后溶液温度的变化情况.