题目内容
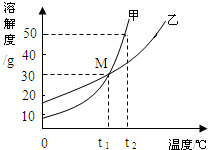 甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )| A、t1℃时,甲、乙各30g分别加入70g水中均恰好完全溶解 | B、t1℃时,甲、乙两物质形成的溶液溶质的质量分数相等 | C、t2℃时,在l00g水中放入60g甲,所得溶液溶质的质量分数为37.5% | D、t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和 |
分析:A、根据某一温度时溶解度的定义考虑本题;B、根据饱和溶液中溶质质量分数的计算方法来考虑;C、60g甲物质并没有全溶解,溶进去的才算溶液的质量;D、在曲线图中从一点降温是向左运动,再根据:曲线上的点和曲线上面的点都是该物质的饱和状态,曲线下面的点属于该物质的不饱和状态进行分析.
解答:解:A、t1℃时,甲和乙的溶解度都是30g,是指在100g水中达到饱和溶解的质量是30g,所以将30g溶于70g水中并不能全溶解,故A错误;
B、饱和溶液的质量分数与溶解度有关,又因为t1℃时,甲和乙的溶解度都是30g,所以t1℃时,甲和乙的饱和溶液溶质质量分数相等,但甲、乙两物质形成的溶液不一定是饱和溶液,所以质量分数不一定相等.故B错;
C、由于t2℃时,甲的溶解度为50g,所以在l00g水中放入60g甲,没有全部溶解,只是溶解了50g,所以质量分数为:
×100%=33.3%,故C错;
D、从溶解度20g向右作平行线,再从t2℃向上作垂线与平行线的交点,向左移动先接触哪一曲线,哪一物质先达到饱和,所以甲先达到饱和,故D正确.
故选D.
B、饱和溶液的质量分数与溶解度有关,又因为t1℃时,甲和乙的溶解度都是30g,所以t1℃时,甲和乙的饱和溶液溶质质量分数相等,但甲、乙两物质形成的溶液不一定是饱和溶液,所以质量分数不一定相等.故B错;
C、由于t2℃时,甲的溶解度为50g,所以在l00g水中放入60g甲,没有全部溶解,只是溶解了50g,所以质量分数为:
| 50g |
| 150g |
D、从溶解度20g向右作平行线,再从t2℃向上作垂线与平行线的交点,向左移动先接触哪一曲线,哪一物质先达到饱和,所以甲先达到饱和,故D正确.
故选D.
点评:通过回答本题知道了溶解度曲线表示的意义,知道了溶解度如何比较大小,饱和溶液溶质质量分数的计算方法,一定质量的物质加入水中,如果不溶解的就不能算溶液的质量.在算溶质质量分数时不溶解的不能算溶液质量.

练习册系列答案
相关题目
根据下表的数据判断,下列有关说法正确的是( )
| 温度 物质 |
0℃ | 20℃ | 30℃ | 50℃ | 80℃ |
| 甲 | 13.3g | 31.6g | 36.2g | 85.8g | 169g |
| 乙 | 35.7g | 36.0g | 36.2g | 36.5g | 37.1g |
| A、甲的溶解度大于乙的溶解度 |
| B、升高温度可把甲的不饱和溶液变为饱和溶液 |
| C、在溶解度曲线图上,甲、乙两物质的溶解度曲线在30℃时相交,此时甲、乙两种物质饱和溶液的溶质质量分数均为26.6% |
| D、使乙物质从它的一定温度下的饱和溶液中析出,一般采用冷却法 |


 (2011?南岗区一模)如图所示为甲、乙两物质的溶解度曲线.20℃时,取甲、乙两种物质(均不含结晶水)各30g,分别加入到100g水中,使之充分溶解,得到相应的混合物.下列有关说法不正确的是( )
(2011?南岗区一模)如图所示为甲、乙两物质的溶解度曲线.20℃时,取甲、乙两种物质(均不含结晶水)各30g,分别加入到100g水中,使之充分溶解,得到相应的混合物.下列有关说法不正确的是( ) (2011?绥化)甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示.下列说法正确的是( )
(2011?绥化)甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示.下列说法正确的是( )