题目内容
【题目】化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应.
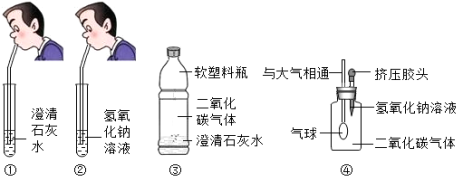
同学们在吹气后观察到①中澄清石灰水边浑浊,②中氢氧化钠溶液无明显现象.观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用 ,针对②中的情况,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中 .
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是 .
(3)小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
取③实验后的溶液少许,再向其加入 ( ) | 验证了二氧化碳和氢氧化钠溶液反应 |
【实验结论】二氧化碳和氢氧化钠溶液发生了化学反应.
【反思拓展】探究结束老师说,通过此探究实验我们发现,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,这些角度可以是:
①通过检验反应物减少证明反应发生;②通过 证明反应的发生.
【答案】澄清的石灰水;【实验探究】(1)气球变大(合理说法均可);(2)将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比;
(3)
实验步骤 | 实验现象 | 实验结论 |
取③实验后的溶液少许,再向其加入 稀盐酸(或氯化钙溶液等) | 有气泡产生(或有白色沉淀生成等) | 验证了二氧化碳和氢氧化钠溶液反应 |
【反思拓展】检验生成物.
【解析】
试题分析:二氧化碳能使澄清石灰水变浑浊,因此可用澄清石灰水来检验二氧化碳;【实验探究】(1)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,瓶内气体减少,气压减小,大气压将空气压入气球,所以气球变大;(2)二氧化碳能与水反应或溶于水,也能使容器内气体减少,压强减小,所以小华的设计不严密,要验证二氧化碳与氢氧化钠溶液确实发生了反应,还需设计对比实验,将氢氧化钠溶液换成等体积的水,再重复实验与放入氢氧化钠溶液的现象(软塑料瓶变瘪的程度是否相同、气球膨胀的大小是否相同)通过对比推导出正确的结论;(3)证明二氧化碳与氢氧化钠溶液发生反应,还可以检验其反应生成物来验证,可向实验后的溶液中滴加稀盐酸或氯化钙溶液,若观察到有气泡生成或白色沉淀生成,说明二者发生了反应,因为氢氧化钠与盐酸反应生成水,无气体生成,氢氧化钠与氯化钙溶液不反应;【反思拓展】通过以上实验可以看出,对于没有明显现象的化学反应,我们可以通过检验反应物是否减少或检验生成物的方法验证反应是否发生;

 小学教材全测系列答案
小学教材全测系列答案【题目】FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
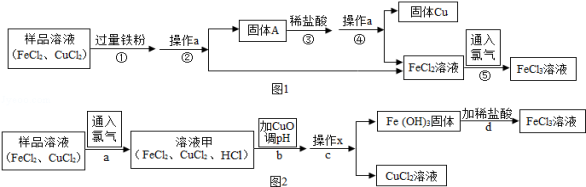
实验一:(如图1)
(1)写出步骤①中发生的化学方程式 ,此反应的基本类型是 .
(2)步骤②中的操作a名称是 ;步骤③中加入稀盐酸的目的是 .
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
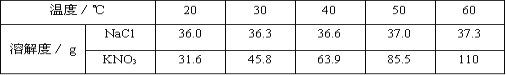
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.7 |
沉淀完全的pH | 3.2 | 6.7 |
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整: , ,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH.
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
【题目】某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
你认为可能还与_________________________________有关(写一条即可)。
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
1.将NaOH溶液加热煮沸 | 溶液变红,过一会儿红色消失 | 甲同学猜想_______(填“正确”或不正确”) | |
2.向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 |
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH溶液反应的化学方程式:________________________。甲同学认为乙同学的实验不够严谨,理由是__________________________________________________。

[注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。]
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH1溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察下图回答问题。
①写出两条规律性结论:_____________________;____________________。

②推测5%的NaOH溶液滴加2滴酚酞试液后褪为无色的时间约为( )
A.小于30s
B.30-90s
C.90-140s
D.140-180s
E.180-280s
F.大于280s