题目内容
小刚收集到一瓶浑浊的太湖水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下所示。请回答以下问题。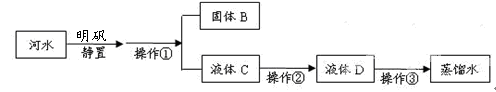
(1)操作①的名称是 。
(2)操作②向滤液C中加入_________,利用其吸附性除去水样中的颜色和异味。此过程主要发生 变化(填“物理”、“化学”)。
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多泡沫出现,说明液体D是 (填“硬水”、“软水”)。
(4)消毒剂高铁酸钠(化学式为Na2FeO4)集氧化、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为 。
(1)操作①的名称是过滤
(2)操作②向滤液C中加入活性炭。此过程主要发生物理变化。
(3)说明液体D是软水。
(4)高铁酸钠中铁元素的化合价为 +6价 。
解析试题分析(1)根据自来水的净化过程可知;①是过滤;(2)活性炭具有蔬松多孔的结构,因此具有吸附性,用活性炭除去一些异味和色素时,没有生成新的物质是物理变化。(3)区分硬水和软水的方法是用肥皂水,加肥皂水时,发现有较多泡沫出现,说明液体是软水。(4)根据化合物元素的正负化合价的代数和为零 (+2)*2+X +(-2)*4="0" 即 X= +6
考点:水的净化,化学式的计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
请从下列物质中选择适当的物质填空:(填字母,下同)
| A.肥皂水 | B.氧气 | C.氢气 | D.明矾 |
(3)常用于区分硬水与软水的是 ; (4)常用净水剂是 。
某公司研制出了一种新颖的“装饰树”,下表为该产品介绍。
| 产品介绍 |
| “装饰树”表面涂了一层光触媒,这种光触媒是一种纳米级二氧化钛,能产生强烈的降解功能,能有效降解空气中的有毒有害气体,如甲醛、一氧化氮、二氧化硫、一氧化碳等。在降解过程中光触媒不挥发,不消耗,具有长效性。 |
(1)根据产品介绍可判断降解反应中二氧化钛是一种 (填“反应物”、“生成物”或“催化剂”)。
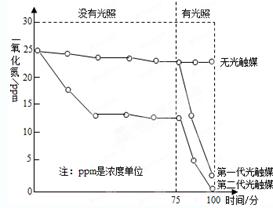
(2)上图是某科研小组探究两代光触媒降解一氧化氮的实验结果,由此可知:
①第一代光触媒产生强烈的降解作用的条件是 ;
②第二代光触媒与第一代光触媒相比,优点是 (写出一点即可)。
 化学基础知识是学好化学的关键,请用化学符号填空:
化学基础知识是学好化学的关键,请用化学符号填空: