题目内容
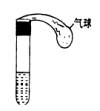
如下图所示,在试管和小气球中分别先加入稀硫酸和一种常见的固体物质,然后将气球中的固体倒入试管中,观察到有气泡产生且气球膨胀变大.请根据上述实验回答下列问题: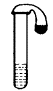
(1)气球中加入的固体物质可能是(答出两种不同种类的物质):
____________________________________________________________
(2)请设计简单的实验,证明制得气体的密度比空气大还是小.
答案:
解析:
提示:
解析:
| 答案:(1)锌粒(或铁屑等) 碳酸钠(或 (2)将胀大的气球取下,并扎紧气球口.若胀大的气球能够在空气中上升,则证明所收集气体的密度比空气小;反之比空气大.(用产生的气体吹肥皂泡,若肥皂泡上升,则气体密度比空气小;反之则大.其他正确方法也可)
|
提示:

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

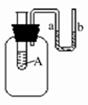
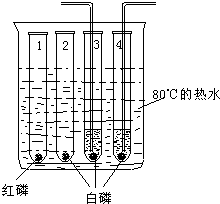 28、为了探究可燃物的燃烧条件,第2实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃.然后他们利用如右图所示的装置进行实验:
28、为了探究可燃物的燃烧条件,第2实验小组的同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃.然后他们利用如右图所示的装置进行实验: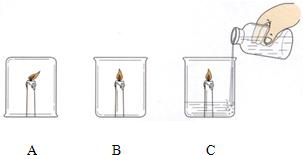

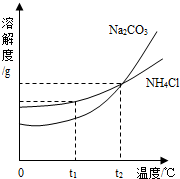 (3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题:
(3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题: