题目内容
【题目】某气体可能含有H2、CO、CO2和CH4四种气体中的一种或几种,为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应和吸收) 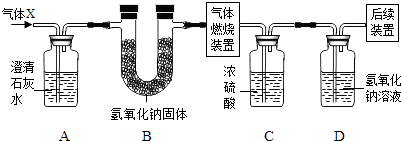
实验过程中装置A无明显变化;实验结束后装置C中增重5.4g,装置D中增重6.6g.
(1)装置B在该实验中的作用是 .
(2)装置D中发生反应的化学方程式为 .
(3)该气体可能的组成有(填序号). ①CH4②CH4和H2③CH4和CO2④CH4和CO ⑤H2和CO ⑥CH4、H2和CO
【答案】
(1)吸收水蒸气
(2)2NaOH+CO2=Na2CO3+H2O
(3)①⑤⑥
【解析】解:二氧化碳能使澄清石灰水变浑浊,实验过程中装置A无明显变化,说明不含有二氧化碳气体;氢氧化钠固体可以吸收空气水蒸气,而浓硫酸具有吸水性,所以实验结束后装置C中增重5.4g就是生成水的质量,氢氧化钠溶液吸收二氧化碳,装置D中增重6.6g就是生成二氧化碳的质量,所以气体中碳元素和氢元素的质量比=(6.6g× ![]() ×100%):(5.4g×
×100%):(5.4g× ![]() ×100%)=3:1,而CH4中碳元素和氢元素的质量比=12:(4×1)=3:1,所以该气体可能的组成有CH4或H2和CO或CH4、H2和CO.(1)装置B在该实验中的作用是吸收水蒸气.(2)装置D中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.(3)该气体可能的组成有CH4或H2和CO或CH4、H2和CO.所以答案是:(1)吸收水蒸气;(2)2NaOH+CO2=Na2CO3+H2O;(3)①⑤⑥.
×100%)=3:1,而CH4中碳元素和氢元素的质量比=12:(4×1)=3:1,所以该气体可能的组成有CH4或H2和CO或CH4、H2和CO.(1)装置B在该实验中的作用是吸收水蒸气.(2)装置D中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.(3)该气体可能的组成有CH4或H2和CO或CH4、H2和CO.所以答案是:(1)吸收水蒸气;(2)2NaOH+CO2=Na2CO3+H2O;(3)①⑤⑥.
【考点精析】通过灵活运用书写化学方程式、文字表达式、电离方程式,掌握注意:a、配平 b、条件 c、箭号即可以解答此题.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目