题目内容
某校小张、小明、小许三位同学在帮化学实验员整理 药品时,发现药品包装箱里有两瓶化学药品的标签已脱落,从脱落的标签可知,这两瓶药品是碳酸钠和碳酸氢钠。为确定这两瓶药品到底哪一瓶是碳酸钠,哪一瓶是碳酸氢钠,三位同学开始了探究行动:
药品时,发现药品包装箱里有两瓶化学药品的标签已脱落,从脱落的标签可知,这两瓶药品是碳酸钠和碳酸氢钠。为确定这两瓶药品到底哪一瓶是碳酸钠,哪一瓶是碳酸氢钠,三位同学开始了探究行动:
[上网查阅资料]资料摘要如下:
碳酸钠是白色粉末或细粒,加热至8 51 ℃时熔化而不分解。Na2CO3易溶于水,其水溶液呈碱性。…… , 碳酸钠的最大用途是制玻璃,也是造纸、肥皂、洗涤剂、纺织、制革、石油、染料、食品等工业的重要原料。
51 ℃时熔化而不分解。Na2CO3易溶于水,其水溶液呈碱性。…… , 碳酸钠的最大用途是制玻璃,也是造纸、肥皂、洗涤剂、纺织、制革、石油、染料、食品等工业的重要原料。
NaHCO3是白色粉末,在水中的溶解度比碳酸钠略小,水溶液呈微碱性,固体碳酸氢钠受热即分解,生成碳酸钠、二氧化碳和水,……,NaHCO3是发酵粉的主要成分,也用于制灭火剂、焙粉或清凉饮料等方面的原料,在橡胶工业中作发泡剂。
[实验方案及探究]根据以上信息及学过的知识,三位同学各自设计的实验方案及探究过程如下。填写下列空白。
[小张同学] 实验方案:将碳酸钠、碳酸氢钠分别溶于水,根据溶液的PH鉴别出两种药品
结论及讨论:(1)小张同学测出两种溶液PH分别为10和8,则PH为10的是 溶液。
(2)水溶液呈碱性的物质一定是碱吗? (填 “是”或“不是”)。
 [小明同学]实验方案:将碳酸钠、碳酸氢钠分别与盐酸发生反应,根据是否有气体生成鉴别出两种药品
[小明同学]实验方案:将碳酸钠、碳酸氢钠分别与盐酸发生反应,根据是否有气体生成鉴别出两种药品
问题讨论:你认为小明同学的实验方案 (填“正确”或“不正确” ),理由是(用化学方程式表示) 。
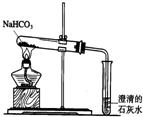
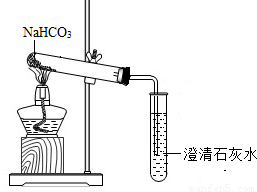
[小许同学]实验方案:根据碳酸钠、碳酸氢钠加热是否分解及生成的产物鉴别出两种药品
实验装置:如右图(图中显示的是加热NaHCO3的情况)
探究报告:小许同学设计的探究报告如下,请你帮他补充完整。
| 实验操作 | 实验现象 | 得出结论 |
[小张同学]
(1)碳酸钠 (1分)。
(2)不是 (1分)。
[小明同学]
不正确(1分), Na2CO3+2HCl ==2NaCl + CO2↑+ H2O、 NaHCO3+HCl == NaCl + CO2↑+H2O (注:本空要写两个化学方程式,共2分,每个化学方程式1分)。
[小许同学]
| 实验操作 | 实验现象 | |
| 分别取少量固体于大试管中,加热,将产生的气体通入装有澄清石灰水的试管中。(1分) | 加热过程中,可看到一种药品产生的气体能使澄清石灰水变浑浊,另一种药品无明显现象。(1分) | 能使澄清石灰水变浑浊的原固体是碳酸氢钠,无明显现象的原固体是碳酸钠。(1分) |

 种药品
种药品