题目内容
氢气是一种热值高的清洁能源,也是重要的化工原料.(1)写出在加热条件下,H2与二氧化锗(GeO2)反应制备金属的化学方程式: .
(2)如何大量、廉价地制备氢气是各国下努力研究的课题.日本科学家最近开发出一种含镍氧化物半导体粉末,将少量这种粉末放入水中,用波长为402nm的可见光照射,能够不断地将水分解成氢气和氧气.在上述过程中,这种氧化物粉末的作用是 ;写出该反应的化学方程式: .
【答案】分析:书写化学方程式时必须根据题意找出反应物、生成物和反应条件,书写时必须遵守质量守恒定律、依据客观事实.
解答:解:(1)根据质量守恒定律中元素种类不变的特点可知:氢气与三氧化二锗在加热条件下反应除生成锗外,还生成水.该反应的化学方程式为:2H2+GeO2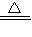 Ge+2H2O.
Ge+2H2O.
②根据题意,该反应是利用水的分解生成氢气和氧气,也就是说含镍氧化物未参加反应只是起到了催化作用.水在含镍氧化物的催化作用和光照下反应生成氢气和氧气.该反应的化学方程式为:2H2O 2H2↑+O2↑.
2H2↑+O2↑.
故答案为:(1)2H2+GeO2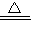 Ge+2H2O;(2)催化作用;2H2O
Ge+2H2O;(2)催化作用;2H2O 2H2↑+O2↑.
2H2↑+O2↑.
点评:本题有一定难度,主要考查同学们根据新信息灵活运用所学化学方程式的书写方法进行书写化学方程式的能力.
解答:解:(1)根据质量守恒定律中元素种类不变的特点可知:氢气与三氧化二锗在加热条件下反应除生成锗外,还生成水.该反应的化学方程式为:2H2+GeO2
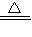 Ge+2H2O.
Ge+2H2O.②根据题意,该反应是利用水的分解生成氢气和氧气,也就是说含镍氧化物未参加反应只是起到了催化作用.水在含镍氧化物的催化作用和光照下反应生成氢气和氧气.该反应的化学方程式为:2H2O
 2H2↑+O2↑.
2H2↑+O2↑.故答案为:(1)2H2+GeO2
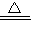 Ge+2H2O;(2)催化作用;2H2O
Ge+2H2O;(2)催化作用;2H2O 2H2↑+O2↑.
2H2↑+O2↑.点评:本题有一定难度,主要考查同学们根据新信息灵活运用所学化学方程式的书写方法进行书写化学方程式的能力.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目