题目内容
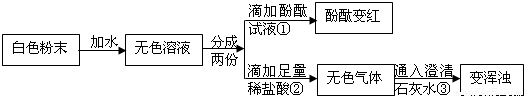
(2007?山西)某同学做实验时发现,盛放NaOH溶液的试剂瓶口与橡皮塞上常有白色粉末出现.为探究这种白色粉末的成分,设计了如下实验.请根据实验完成后面各题.

(1)由实验①可知,无色溶液显
(2)写出实验③中反应的化学方程式
(3)通过上述实验你认为氢氧化钠溶液变质的原因是

(1)由实验①可知,无色溶液显
碱
碱
性;由实验②③可知,氢氧化钠变质后生成的白色粉末中一定含有的物质是Na2CO3
Na2CO3
(填化学式).(2)写出实验③中反应的化学方程式
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.(3)通过上述实验你认为氢氧化钠溶液变质的原因是
与空气中的CO2反应(或2NaOH+CO2═Na2CO3+H2O)
与空气中的CO2反应(或2NaOH+CO2═Na2CO3+H2O)
;你认为该实验方案有何不足?没有检验出白色粉末中是否含有NaOH
没有检验出白色粉末中是否含有NaOH
.分析:固体氢氧化钠易潮解,潮解后与二氧化碳反应,同样氢氧化钠溶液本身更容易和空气中的二氧化碳反应而生成碳酸钠.
解答:解:(1)实验①中酚酞试液变红可知溶液呈碱性而实验②中滴加稀盐酸后产生气体,可知氢氧化钠已变质产生了碳酸钠,因为氢氧化钠和盐酸反应不会产生气体,实验③进一步证明了上述结论所以本题答案为:碱 Na2CO3
(2)由(1)中所分析的那样,实验③中所发生的正是二氧化碳和氢氧化钙的反应,其化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O
(3)根据实验现象我们可知白色固体中有碳酸钠,而碳酸钠在这里只能由氢氧化钠与二氧化碳反应得到,但是在本实验方案中没有涉及到的是:白色固体中是不是含有氢氧化钠这是本实验方案的不足之处.本题答案为:与空气中的CO2反应(或2NaOH+CO2═Na2CO3+H2O) 没有检验出白色粉末中是否含有NaOH
(2)由(1)中所分析的那样,实验③中所发生的正是二氧化碳和氢氧化钙的反应,其化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O
(3)根据实验现象我们可知白色固体中有碳酸钠,而碳酸钠在这里只能由氢氧化钠与二氧化碳反应得到,但是在本实验方案中没有涉及到的是:白色固体中是不是含有氢氧化钠这是本实验方案的不足之处.本题答案为:与空气中的CO2反应(或2NaOH+CO2═Na2CO3+H2O) 没有检验出白色粉末中是否含有NaOH
点评:本题主要就是考查氢氧化钠变质及怎样检验氢氧化钠是否变质的方法,只要掌握了碳酸盐的检验方法,解答本题就很容易了.

练习册系列答案
相关题目