题目内容
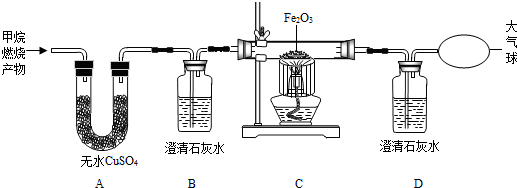
现拟用如图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜粉样品(混有CuO粉末)中金属铜的含量.
(1)制备一氧化碳的化学方程式是______;
(2)实验中,观察到反应管中发生的现象是______,
尾气的主要成分是______;
(3)反应完成后,正确的操作顺序为______(填字母);
a.关闭漏斗开关b.熄灭酒精灯1c.熄灭酒精灯2
(4)若实验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为______;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案:
①设计方案的主要步骤是(不必描述操作过程的细节)______;
②写出有关反应的化学方程式______.

(1)制备一氧化碳的化学方程式是______;
(2)实验中,观察到反应管中发生的现象是______,
尾气的主要成分是______;
(3)反应完成后,正确的操作顺序为______(填字母);
a.关闭漏斗开关b.熄灭酒精灯1c.熄灭酒精灯2
(4)若实验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,则原样品中单质铜的质量分数为______;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样品中金属铜质量分数的方案:
①设计方案的主要步骤是(不必描述操作过程的细节)______;
②写出有关反应的化学方程式______.

(1)甲酸在浓硫酸、加热的条件下分解生成CO与H2O,反应方程式为HCOOH
CO↑+H2O;
故答案为:HCOOH
CO↑+H2O;
(2)实验中,反应管中发生反应CuO+CO
Cu+CO2,反应管中发生的现象是黑色粉末变红;尾气的主要成分是CO、CO2;
故答案为:样品由黑色变红色;CO、CO2;
(3)反应完后,操作顺序先撤酒精灯2,此时左边装置仍在制取CO,然后再关闭分液漏斗的开关,不再加入反应试剂,最后撤酒精灯1停止反应,这样操作防止空气中O2进入右边装置铜又被氧化为氧化铜了,正确的操作顺序为:熄灭酒精灯2,关闭漏斗开关,最后熄灭酒精1,即cab;
故答案为:cab;
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,剩余固体全部为铜,令样品中CuO的质量为m,则:
CuO+CO
Cu+CO2,固体质量减少△m
80 16
m 5g-4.8g=0.2g
=
故m=1g,
所以原样品中金属铜的质量分数为
×100%=80%;
故答案为:80%;
(5)①要测定铜的质量分数,可以把浓硫酸稀释,铜和稀硫酸不反应,氧化铜和稀硫酸反应,即可求出铜的质量分数.设计方案的主要步骤是将浓硫酸用蒸馏水稀释,将样品与稀硫酸充分反应后,过滤,干燥,称量剩余固体铜的质量即可;
故答案为:将浓硫酸稀释;称取一定量的样品;样品与过量稀硫酸充分反应;过滤、洗涤;干燥、称重、计算;
②反应的化学方程式为CuO+H2SO4═CuSO4+H2O.
故答案为:CuO+H2SO4═CuSO4+H2O.
| ||
| △ |
故答案为:HCOOH
| ||
| △ |
(2)实验中,反应管中发生反应CuO+CO
| ||
故答案为:样品由黑色变红色;CO、CO2;
(3)反应完后,操作顺序先撤酒精灯2,此时左边装置仍在制取CO,然后再关闭分液漏斗的开关,不再加入反应试剂,最后撤酒精灯1停止反应,这样操作防止空气中O2进入右边装置铜又被氧化为氧化铜了,正确的操作顺序为:熄灭酒精灯2,关闭漏斗开关,最后熄灭酒精1,即cab;
故答案为:cab;
(4)若试验中称取铜粉样品5.0g,充分反应后,反应管中剩余固体的质量为4.8g,剩余固体全部为铜,令样品中CuO的质量为m,则:
CuO+CO
| ||
80 16
m 5g-4.8g=0.2g
| 80 |
| m |
| 16 |
| 0.2g |
故m=1g,
所以原样品中金属铜的质量分数为
| 5g-1g |
| 5g |
故答案为:80%;
(5)①要测定铜的质量分数,可以把浓硫酸稀释,铜和稀硫酸不反应,氧化铜和稀硫酸反应,即可求出铜的质量分数.设计方案的主要步骤是将浓硫酸用蒸馏水稀释,将样品与稀硫酸充分反应后,过滤,干燥,称量剩余固体铜的质量即可;
故答案为:将浓硫酸稀释;称取一定量的样品;样品与过量稀硫酸充分反应;过滤、洗涤;干燥、称重、计算;
②反应的化学方程式为CuO+H2SO4═CuSO4+H2O.
故答案为:CuO+H2SO4═CuSO4+H2O.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
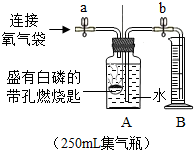 实验记录:
实验记录: