题目内容
实验室中有一瓶氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质.化学课外兴趣小组的同学决定测定该瓶试剂变质的程度,他们根据所学知识,依次进行了如下的实验操作:①取该瓶中的试剂30g加水配制成溶液A;②向溶液A中加入足量澄清的石灰水;③过滤、干燥、称量,得到4g白色沉淀.
试回答下列问题:
(1)叙述氢氧化钠固体敞口放置变质的原因是 .
(2)若向上述变质的氢氧化钠固体中加入足量的稀盐酸,能观察到的一个明显现象是 .
(2)写出溶液A中的溶质(填化学式) .
(3)计算该30g试剂中含有杂质Na2CO3的质量分数(最终结果精确到0.1%).
| 氢氧化钠固体易吸收空气中的二氧化碳形成碳酸钠而变质,所以部分变质的氢氧化钠为氢氧化钠和碳酸钠形成的混合物,碳酸钠会和盐酸反应产生二氧化碳;根据碳酸钠与氢氧化钙反应的化学方程式,由生成沉淀碳酸钙的质量计算样品中碳酸钠的质量,该质量与样品的质量比可计算含有杂质Na2CO3的质量分数. | |
| 解答: | 解:(1)氢氧化钠固体能吸收空气中二氧化碳形成碳酸钠而变质; (2)变质后含有碳酸钠会和盐酸反应产生二氧化碳,会观察到有气泡产生; (3)部分变质的氢氧化钠为氢氧化钠与碳酸钠的混合物,则溶液中含有碳酸钠、氢氧化钠(Na2CO3、NaOH); (4)设碳酸钠的物质的质量为x Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 106 100 x 4g
答:30g试剂中含有杂质Na2CO3的质量分数是14.1%. 故答案为:(1)氢氧化钠在空气中会与空气中的二氧化碳反应生成碳酸钠;(2)有气泡产生;(3)Na2CO3、NaOH;(4)14.1%. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 =
= x=4.24g则碳酸钠的质量分数=
x=4.24g则碳酸钠的质量分数= ×100%=14.1%
×100%=14.1% 28、实验室中有一瓶无色液体,经测定其中只含氢、氧两种元素.请你对该无色液体进行如下探究活动,请回答下列问题:
28、实验室中有一瓶无色液体,经测定其中只含氢、氧两种元素.请你对该无色液体进行如下探究活动,请回答下列问题: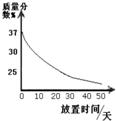


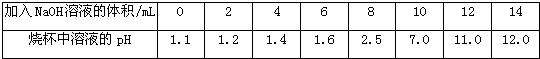
 实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题:
实验室有一瓶氢氧化钾浓溶液,瓶上标签内容如图所示,请你根据签上提供的数据解答下列问题: