题目内容
煤的气化可以提高煤的利用率、减少环境污染.煤的气化过程中发生的化学反应:C+H2O(气)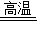 H2+CO,该反应的反应类型是( )
H2+CO,该反应的反应类型是( )A.化合反应
B.分解反应
C.置换反应
D.复分解反应
【答案】分析:化合反应,两种或两种以上物质反应后生成一种物质的反应,其特点可总结为“多变一”;置换反应是一种单质和一种化合物反应生成一种单质和一种化合物;分解反应,一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,复分解反应是两种化合物相互交换成分生成两种新的化合物的反应.
解答:解:反应物一种单质和一种化合物,生成物为一种单质和一种化合物,所以为置换反应.
故选C.
点评:抓住四种反应的特点,根据反应前后物质种类数“多变一”还是“一变多”是单质和化合物还是两种化合物,对所以发生的反应进行类型判断.
解答:解:反应物一种单质和一种化合物,生成物为一种单质和一种化合物,所以为置换反应.
故选C.
点评:抓住四种反应的特点,根据反应前后物质种类数“多变一”还是“一变多”是单质和化合物还是两种化合物,对所以发生的反应进行类型判断.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
 H2+CO,该反应的反应类型是( )
H2+CO,该反应的反应类型是( )