题目内容
我们已经知道,空气的主要成分是氮气和氧气.下图是测定空气中氧气含量的实验装置.试回答下列问题:(1)实验过程中,燃烧匙里为什么要盛放过量的红磷?
______.
(2)这个实验除了可以得出氧气约占空气体积的1/5的结论外,还可推出氮气______(填“易”“难”)溶于水和其化学性质______(填“活泼”“不活泼”)的结论.
(3)在此实验过程中能否用碳、硫代替红磷?______.

【答案】分析:(1)根据测定空气中氧气含量的原理和注意事项回答.
(2)根据红磷熄灭后装置中还有剩余气体,且液面不再变化回答.
(3)根据测定空气中氧气含量的原理和注意事项回答.
解答:解:(1)测定空气中氧气含量的原理是利用磷燃烧只消耗氧气,且不生成新气体,由于氧气被消耗,瓶内气压减小,水倒吸入瓶内,进入水的体积即为空气中氧气的体积.如红磷的量不足,则氧气不能耗尽,进入水的体积小于空气中氧气的实际含量.
(2)红磷红磷熄灭后装置中还有剩余气体,气体主要是氮气,而液面不再变化,说明氮气难溶于水,化学性质不活泼,也不与水发生反应.
(3)在此实验过程中不能用碳、硫代替红磷.因为碳、硫与氧气反应分别生成二氧化碳和二氧化硫气体,不会造成压强差,导致不能等量进入水,从而无法判断空气中氧气的体积.
故答案为:
(1)让O2尽量消耗完全,使测得O2的体积更接近空气中O2的实际体积;
(2)难;不活泼;
(3)不能.
点评:空气是人类宝贵的自然资源,在中考中占有重要的地位,特别是空气中氧气含量的测定,要注意测定原理、实验关键、现象和结论、装置的评价和改进等内容的考查.
(2)根据红磷熄灭后装置中还有剩余气体,且液面不再变化回答.
(3)根据测定空气中氧气含量的原理和注意事项回答.
解答:解:(1)测定空气中氧气含量的原理是利用磷燃烧只消耗氧气,且不生成新气体,由于氧气被消耗,瓶内气压减小,水倒吸入瓶内,进入水的体积即为空气中氧气的体积.如红磷的量不足,则氧气不能耗尽,进入水的体积小于空气中氧气的实际含量.
(2)红磷红磷熄灭后装置中还有剩余气体,气体主要是氮气,而液面不再变化,说明氮气难溶于水,化学性质不活泼,也不与水发生反应.
(3)在此实验过程中不能用碳、硫代替红磷.因为碳、硫与氧气反应分别生成二氧化碳和二氧化硫气体,不会造成压强差,导致不能等量进入水,从而无法判断空气中氧气的体积.
故答案为:
(1)让O2尽量消耗完全,使测得O2的体积更接近空气中O2的实际体积;
(2)难;不活泼;
(3)不能.
点评:空气是人类宝贵的自然资源,在中考中占有重要的地位,特别是空气中氧气含量的测定,要注意测定原理、实验关键、现象和结论、装置的评价和改进等内容的考查.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
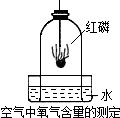 我们已经知道,空气的主要成分是氮气和氧气,下图是测定空气中氧气含量的实验装置,试回答下列问题.
我们已经知道,空气的主要成分是氮气和氧气,下图是测定空气中氧气含量的实验装置,试回答下列问题. 21、我们已经知道,空气的主要成分是氮气和氧气.下图是测定空气中氧气含量的实验装置.试回答下列问题:
21、我们已经知道,空气的主要成分是氮气和氧气.下图是测定空气中氧气含量的实验装置.试回答下列问题: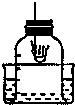
 (1)做铁丝在氧气中燃烧的实验时,把铁丝绕成螺旋状,细铁丝前端系一根火柴,其作用是
(1)做铁丝在氧气中燃烧的实验时,把铁丝绕成螺旋状,细铁丝前端系一根火柴,其作用是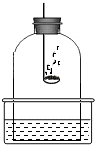 我们已经知道了空气的主要成分是氮气和氧气,右下图为测定空气中氧气含量的实验装置图.
我们已经知道了空气的主要成分是氮气和氧气,右下图为测定空气中氧气含量的实验装置图.