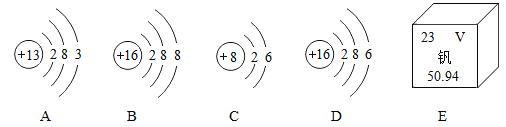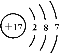题目内容
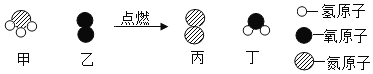
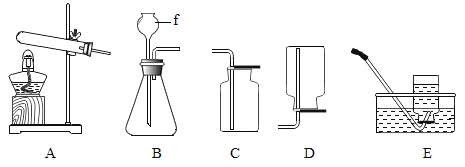
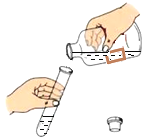
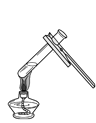
【题目】甲乙两位同学在学完酸碱盐的化学性质之后,分别作了如图所示的实验。
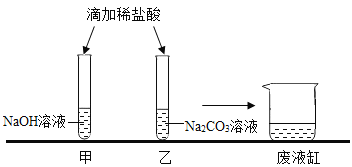
(观察与讨论1)
(1)甲同学实验中没有观察到明显的现象,他认为二者没有发生反应。为证明甲同学试管中的物质能反应,先向NaOH溶液中滴几滴____________________(填指示剂名称)试液,再滴加适量的稀盐酸,当观察到颜色变化时,就可以说明两种物质发生了反应。
(2)乙同学实验中发生反应的化学方程式为_____________________。
(观察与讨论2)实验结束后,甲、乙两位同学依次将各自试管中的废液倒入同一个洁净的废液缸中,形成无色溶液。甲同学取少量废液于试管中,滴入无色酚酞试液,发现溶液呈红色,则该废液中的溶质一定不含_______________________________ (填化学式)。
为了科学处理废液,两位同学决定对废液缸中最终的废液进行探究。
(提出问题)最终废液中除含NaCl外,还含有其它什么溶质?
(作出猜想)猜想I:还含有Na2CO3;
猜想Ⅱ:还含有NaOH;
猜想Ⅲ:还含有_______________________。
(进行实验)甲同学的实验过程如表所示,请你完成如表所示的实验报告:(已知CaCl2溶液呈中性)
实验步骤 | 实验现象 | 实验结论 |
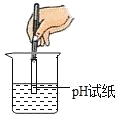
1.测定废液的pH | pH>7 | 废液中含有NaOH |
2.取少量废液于试管中,加入过量氯化钙溶液,再滴入无色酚酞试液 | ___________________ | 猜想Ⅲ成立 |
(反思与交流)乙同学认为甲同学步骤1的结论不正确,原因是______________。
【答案】酚酞或紫色石蕊 2HCl+Na2CO3=2NaCl+H2O+CO2↑ HCl Na2CO3、NaOH 有白色沉淀产生,废液由无色变为红色 碳酸钠溶液显碱性,pH也大于7
【解析】
[观察与讨论1](1)为证明甲同学试管中的物质能反应,先向NaOH溶液中滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到溶液由红色变成无色时,说明氢氧化钠已经完全反应,进一步说明两种物质发生了反应。故填:酚酞试液;
(2)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳;故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
[观察与讨论2]甲同学取少量废液于试管中,滴入无色酚酞试液,发现溶液呈红色,则该废液中的溶质一定不含氯化氢,这是因为盐酸显酸性,不能使酚酞试液变色。故填:HCl;
[作出猜想]猜想Ⅰ:还含有Na2CO3;
猜想Ⅱ:还含有NaOH;
猜想Ⅲ:还含有Na2CO3、NaOH。
故填:Na2CO3、NaOH。
[进行实验]
1、测定废液的pH,pH>7,说明溶液显碱性;
2、取少量废液于试管中,向试管中加入过量氯化钙溶液,再滴入无色酚酞试液,有白色沉淀产生,无色酚酞试液变红色,说明溶液中含有氢氧化钠和碳酸钠,实验过程如下所示:
实验步骤 | 实验现象 | 实验结论 |
1、测定废液的pH | pH>7 | 废液中含有NaOH |
2、取少量废液于试管中,向试管中加入过量氯化钙溶液,再滴入无色酚酞试液。 | 有白色沉淀产生,无色酚酞试液变红色 | 猜想Ⅲ成立 |
故填:有白色沉淀产生,无色酚酞试液变红色;
[反思]乙同学认为甲同学步骤1结论不正确,原因是碳酸钠溶液显碱性,pH>7.故填:碳酸钠溶液显碱性,pH>7。

 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】甲、乙、丙三种物质的转化关系如下图所示(“→”表示反应能一步实现, 部分反应物、生成物和反应条件均已略去),下列选项不能实现图示转化的是
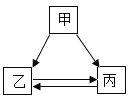
甲 | 乙 | 丙 | |
A | C | CO | CO2 |
B | Na2CO3 | CO2 | CaCO3 |
C | H2SO4 | CuSO4 | Cu(OH)2 |
D | H2O2 | H2O | O2 |
A.AB.BC.CD.D
【题目】化学语言是学习化学的重要工具。
(1) 完成下列化学反应的符号表达式:
化学反应 | 符号表达式 |
红磷在氧气中燃烧 | ①__________________ |
木炭在氧气中燃烧 | ②_____________ |
(2)填写化学符号或化学符号表示的含义:
内容 | ③ | ④ | ⑤ | |
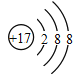
化学符号 | 2Fe | ____ | ______ |
|
表示含义 | ______ | 1个钠离子 | 1个氯离子 | 最外层电子数为____,属于____元素(填“金属”或“非金属”)。 |