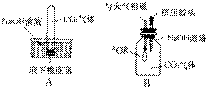题目内容
28、某化学兴趣小组同学发现铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.他们通过实验探究,分析黑色粉末的组成.
(1)提出问题:黑色固体是什么?
(2)猜想与假设:甲、乙、丙三位同学各自提出不同的假设,分别猜想黑色固体的组成:甲认为可能是炭粉(一种碳的单质);乙认为可能是氧化铜;丙认为可能是炭粉和氧化铜的混合物.
三位同学中有一位的假设因为不合理,被另两位同学予以否定,请问是哪一位?不合理的原因是
(3)查阅资料:氧化铜和炭粉均为黑色固体,其中氧化铜可与稀酸反应而溶解,炭粉不与稀酸反应,也不溶于稀酸.
(4)设计实验方案:验证另外两位同学的假设.
向试管中的黑色固体滴加足量的
(5)现象和结论:
若现象为
若现象为
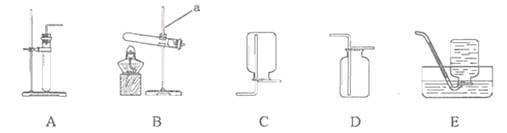
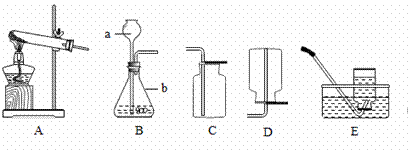
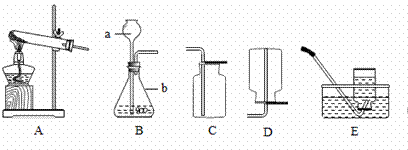
(6)如图为实验室用CO还原CuO的装置图,图中浓硫酸的作用是

(1)提出问题:黑色固体是什么?
(2)猜想与假设:甲、乙、丙三位同学各自提出不同的假设,分别猜想黑色固体的组成:甲认为可能是炭粉(一种碳的单质);乙认为可能是氧化铜;丙认为可能是炭粉和氧化铜的混合物.
三位同学中有一位的假设因为不合理,被另两位同学予以否定,请问是哪一位?不合理的原因是
甲同学.因为在他的结论中没有铜元素,根据质量守恒定律,反应前后元素种类不变,因此是错误的
.(3)查阅资料:氧化铜和炭粉均为黑色固体,其中氧化铜可与稀酸反应而溶解,炭粉不与稀酸反应,也不溶于稀酸.
(4)设计实验方案:验证另外两位同学的假设.
向试管中的黑色固体滴加足量的
稀盐酸或稀硫酸
溶液,待充分反应后,观察固体的溶解情况和所得溶液的颜色.(5)现象和结论:
若现象为
固体全部溶解且溶液变为蓝色
,则乙
同学猜想正确;若现象为
固体部分溶解且溶液变为蓝色
,则丙
同学假设成立.(6)如图为实验室用CO还原CuO的装置图,图中浓硫酸的作用是
对生成的二氧化碳气体进行干燥
,装置E中应放入的药品是NaOH
(填化学式),反应后必须对尾气进行处理的原因是:防止一氧化碳污染空气
.
分析:(2)根据题意铜绿[Cu2(OH)2CO3]受热分解后,生成CO2和水蒸气,可根据质量守恒定律来判断黑色物质的组成.
(4)可根据碳和氧化铜的化学性质进行分析,碳的性质比较稳定,氧化铜可以溶于酸.
(5)可根据碳不溶于酸,而氧化铜可以和酸反应而溶解,且溶液为蓝色进行分析解答.
(6)可根据碳和二氧化碳反应必须在干燥的试管中反应进行分析浓硫酸的作用;根据碳还原氧化铜反应是通过生成的二氧化碳气体与G装置反应,产生浑浊来证明进行分析E装置中的试剂.
(4)可根据碳和氧化铜的化学性质进行分析,碳的性质比较稳定,氧化铜可以溶于酸.
(5)可根据碳不溶于酸,而氧化铜可以和酸反应而溶解,且溶液为蓝色进行分析解答.
(6)可根据碳和二氧化碳反应必须在干燥的试管中反应进行分析浓硫酸的作用;根据碳还原氧化铜反应是通过生成的二氧化碳气体与G装置反应,产生浑浊来证明进行分析E装置中的试剂.
解答:解:(2)根据题意铜绿[Cu2(OH)2CO3]受热分解后,生成CO2和水蒸气,根据质量守恒定律可知黑色固体中必定含有铜元素,甲同学的猜想中没有铜元素,所以甲同学猜想错误.
故答案为:甲同学.因为在他的结论中没有铜元素,根据质量守恒定律,反应前后元素种类不变,因此是错误的;
(4)因为碳的性质比较稳定,氧化铜可以可溶于酸,且生成可溶性铜盐的溶液呈蓝色,所以可用酸来鉴别.
故答案为:稀盐酸或稀硫酸;
(5)因为碳不溶于酸,而氧化铜可以溶于稀硫酸中,溶液变为蓝色的硫酸铜溶液,所以如果乙同学正确,则固体全部溶解且溶液呈蓝色,若丙同学正确,固体将是部分溶解.
故答案为:固体全部溶解且溶液变为蓝色;乙;
固体部分溶解且溶液变为蓝色;丙;
(6)碳和二氧化碳反应必须在干燥的试管中反应进行,若二氧化碳气体中含有水蒸气,试管可能破裂,所以浓硫酸的作用是干燥二氧化碳气体;
证明碳还原氧化铜是通过生成的二氧化碳气体可以使澄清石灰水变浑浊,所以必须对生成的CO中的二氧化碳除去,通常采用氢氧化钠溶液来吸收二氧化碳.
CO有毒,会污染气体,实验室一般采用点燃的方法除去尾气CO.
故答案为:对生成的二氧化碳气体进行干燥; NaOH;防止一氧化碳污染空气.
故答案为:甲同学.因为在他的结论中没有铜元素,根据质量守恒定律,反应前后元素种类不变,因此是错误的;
(4)因为碳的性质比较稳定,氧化铜可以可溶于酸,且生成可溶性铜盐的溶液呈蓝色,所以可用酸来鉴别.
故答案为:稀盐酸或稀硫酸;
(5)因为碳不溶于酸,而氧化铜可以溶于稀硫酸中,溶液变为蓝色的硫酸铜溶液,所以如果乙同学正确,则固体全部溶解且溶液呈蓝色,若丙同学正确,固体将是部分溶解.
故答案为:固体全部溶解且溶液变为蓝色;乙;
固体部分溶解且溶液变为蓝色;丙;
(6)碳和二氧化碳反应必须在干燥的试管中反应进行,若二氧化碳气体中含有水蒸气,试管可能破裂,所以浓硫酸的作用是干燥二氧化碳气体;
证明碳还原氧化铜是通过生成的二氧化碳气体可以使澄清石灰水变浑浊,所以必须对生成的CO中的二氧化碳除去,通常采用氢氧化钠溶液来吸收二氧化碳.
CO有毒,会污染气体,实验室一般采用点燃的方法除去尾气CO.
故答案为:对生成的二氧化碳气体进行干燥; NaOH;防止一氧化碳污染空气.
点评:本题主要通过对铜绿分解产物的探究来考查学生对探究实验设计思路的掌握情况,及有关实验具体操作相关知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目