题目内容
【题目】2019年是元素期表诞生第150周年,下表是元素周期表中第2、3周期的元素。请回答
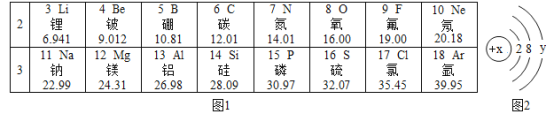
(1)请从图1表中查出关于铝元素的一条信息:_____,其对应的阳离子的符号是____。
(2)下列各组具有相似化学性质的元素是____(填字母序号)。
A Na、Li
B O、S
C F、C1
D C1、Ar
(3)第7号元素与第12号元素的原子形成化合物的化学式为____。
(4)某离子的结构示意图如图2所示,y为非零整数,当x-y=8时,该粒子的符号为_____。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质,下列各组粒子中属于等电子体的是____。(填字母序号)
A Ne和H2O
B CO和N2
C SO2和CO2
D NO和O2
【答案】铝元素的原子序数为13(或:铝元素的元素符号为Al、铝元素的相对原子质量为26.98、铝元素属于金属元素) Al3+ A、B、C Mg3N2 S2- B
【解析】
(1)请从图1表中查出关于铝元素的一条信息:1、铝元素的原子序数为13;2、铝元素的元素符号为Al;3、铝元素的相对原子质量为26.98;4、铝元素属于金属元素;氯原子最外层有三个电子,发生化学反应容易失去3个电子形成铝离子,符号是:Al3+;
(2)
A、Na原子最外层有1个电子,Li最外层有1个电子,最外层电子数相等,化学性质相似;
B、O原子最外层有6个电子,S原子最外层有6个电子,最外层电子数相等,化学性质相似;
C、F原子最外层有7个电子,C1原子最外层有7个电子,最外层电子数相等,化学性质相似;
D、C1最外层有7个电子,Ar最外层有8个电子,最外层电子数不相等,化学性质不相似;
故选:ABC。
(3)第7号元素是氮元素与第12号元素是镁元素,形成化合物是二氮化三镁,化学式为:Mg3N2;
(4)某离子的结构示意图如图2所示,y为非零整数,当x-y=10时,表示原子,当x-y=8时,该粒子得2个电子变为阴离子,硫原子得2个电子变为18电子,最外层电子数为8,符合质子数-最外层电子数=16-8=8,该离子符号为:S2-;
(5) A、1个Ne原子中含有10个电子,1个H2O分子中含有2+8=10个电子,但是原子数不相同,不属于等电子体;
B、1个CO分子中含有6+8=14个电子,1个N2分子中含有2×7=14个电子,属于等电子体;
C、1个SO2分子中含有16+8×2=32个电子,1个CO2分子中含有6+8×2=22个电子,不属于等电子体;
D、1个NO分子中含有7+8=15个电子,1个O2分子中含有8×2=16个电子,不属于等电子体;
故选: B。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()
【题目】为了探究蜡烛(主要含 C、H、O 元素)燃烧后的产物, 利用多功能传感器进行有关量的测量,装置如图所示,

实验结束后,铝板表面有黑色固体颗粒,同时传感器 采得实验前后的有关数据如表所示:
相对湿度 | O2 含量 | CO2 含量 | CO 含量 | |
点燃前 | 48.4% | 18.7% | 0.058% | 0 |
熄灭后 | 71.6% | 15.6% | 3.643% | 0.0182% |
根据实验分析生成的产物有水、CO2、_____和_____。