题目内容
【题目】化学兴趣小组的同学将光亮的镁条插入滴有酚酞的饱和NaHCO3溶液中,产生大量气泡和白色固体,溶液红色加深。某化学兴趣小组同学对这一异常现象产生了兴趣,为探究产生气体的成分和白色固体的成分,他们分组进行了如下实验。
[查阅资料]Mg(OH)2难溶于水,MgCO3微溶于水;MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
探究实验一-:
[提出问题]产生的气体是什么?
[作出猜想]猜想1:H2 猜想2:CO2 猜想3:H2 和CO2
[实验验证]
实验方案 | 实验步骤及现象 | 实验结论 |
① | 收集生成的气体,将气体通入澄清石灰水中,观察到__________________________。 | 猜想2、3不成立 |
② | 收集生成的气体,将气体通过浓硫酸后点燃,气体安静燃烧,火焰呈淡蓝色,在火焰上方罩一个干冷的烧杯,内壁有水雾 | 猜想1成立 |
探究实验二:
[提出问题)生成的白色固体是什么?
[作出猜想]猜想1:MgCO3 猜想 2:Mg(OH)2 猜想3:MgCO3和Mg(OH)2
[实验验证]
实验方案 | 实验步骤 | 实验结论 |
① | 取白色固体加入足量稀盐酸,,有大量气泡生成,产生气泡的化学方程式为_________________。 | 猜想_______________________不成立 |
② | 取白色固体干燥后,充分加热至不再产生气体,将产生的气体先通过碱石灰,再通过浓硫酸,发现碱石灰增重,浓硫酸质量不变 | 猜想1成立 |
[反思交流]
(1)探究实验二中实验方案②将白色固体干燥后再加热的目的是___________________。
(2)其他同学认为探究实验二结论不正确,原因是_________________________,改进方法是_________________________。
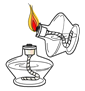
【答案】无明显现象(或澄清石灰水未变浑浊) ![]() 2 排除水对检验氢氧化镁是否存在的干扰 碱石灰能够吸收水和二氧化碳 将产生的气体先通过浓硫酸,再通过碱石灰
2 排除水对检验氢氧化镁是否存在的干扰 碱石灰能够吸收水和二氧化碳 将产生的气体先通过浓硫酸,再通过碱石灰
【解析】
探究实验一
[实验验证]:
①收集生成的气体,将气体通入澄清石灰水中,根据猜想2、3不成立,说明肯定不含二氧化碳,即观察到澄清石灰水未变浑浊或无明显现象。
②将气体通过浓硫酸的作用是利用浓硫酸的吸水性将气体中混有的水分除去,也为检验氢气排除干扰。
探究实验二
[实验验证]:
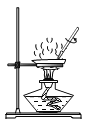
①取白色固体加入足量稀盐酸,有大量气泡生成,说明肯定含有碳酸盐;猜想2不成立,则产生气泡的反应为碳酸镁与盐酸反应生成氯化镁、二氧化碳和水,方程式为:![]() 。
。
②取白色固体干燥后进行实验,根据题给信息“MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物”可知,碳酸镁受热分解为氧化镁和二氧化碳,氢氧化镁受热分解为氧化镁和水,将产生的气体先通入碱石灰,再通入浓硫酸,分别称量装置反应前后的质量。
[反思交流]:
(1)探究实验二中实验方案②要通过检验是否有水生成来判断白色固体中是否有氢氧化镁,所以一定要把白色固体干燥后再加热。
(2)因为碱石灰能够吸收水和二氧化碳,如果白色固体中含有氢氧化镁,受热分解生成的水也能够被碱石灰吸收,从而导致浓硫酸质量不变;改进方法是:将产生的气体先通过浓硫酸,再通过碱石灰,如果白色固体中含有氢氧化镁,则受热分解生成的水能够被浓硫酸吸收。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案