题目内容
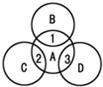 A、B、C、D分别是铁、盐酸、碳酸钠溶液、氢氧化钠溶液中的一种,其反应关系如图所示,图中两圆相交部分1、2、3表示两种物质之间反应的主要现象,其中1无明显现象.请思考下列问题:
A、B、C、D分别是铁、盐酸、碳酸钠溶液、氢氧化钠溶液中的一种,其反应关系如图所示,图中两圆相交部分1、2、3表示两种物质之间反应的主要现象,其中1无明显现象.请思考下列问题:(1)A与D反应的产物之一可作灭火剂,则2的现象是
有气泡产生,溶液由无色变为浅绿色
有气泡产生,溶液由无色变为浅绿色
.(2)A与C反应的化学方程式:
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
,基本反应类型为置换反应
置换反应
,A与D反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑
Na2CO3+2HCl═2NaCl+H2O+CO2↑
.(3)要验证A与D反应得到的气体产物,可将其通入
澄清石灰水
澄清石灰水
中,反应的化学方程式是Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
.分析:由图示可知只有A能与其余三种物质都反应,所给物质中只有盐酸能与其它物质发生反应,铁与盐酸反应生成氯化亚铁和氢气,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,盐酸与氢氧化钠反应生成氯化钠和水,所以A是盐酸,由A与D反应的产物之一可作灭火剂,即产生二氧化碳,所以D是碳酸钠,由其中1无明显现象,可知B是氢氧化钠,所以C是铁,再根据方程式的写法和二氧化碳的鉴别方法,反应类型的鉴别方法考虑.
解答:解:所给物质中只有盐酸能与其它物质发生反应,铁与盐酸反应生成氯化亚铁和氢气,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,盐酸与氢氧化钠反应生成氯化钠和水,由图示可知只有A能与其余三种物质都反应,所以A是盐酸,由于二氧化碳既不能燃烧也不支持燃烧,且密度比空气大,所以可以用来灭火,A与D反应的产物之一可作灭火剂,即产生二氧化碳,所以D是碳酸钠,由其中1无明显现象,可知B是氢氧化钠,因为氢氧化钠与盐酸反应生成氯化钠和水,没有现象.
(1)铁与盐酸反应生成氯化亚铁和氢气,亚铁离子溶液是浅绿色,所以反应现象是:有气泡产生,溶液由无色变为浅绿色;
(2)A与C反应的反应物是铁和盐酸,生成物是氯化亚铁和氢气,用观察法配平,氢气后面标上上升符号;反应物中有一种是单质,有一种是化合物,生成物中有一种是单质,有一种是化合物,所以反应类型是置换反应;A与D反应的反应物是碳酸钠和盐酸,生成物是氯化钠、水和二氧化碳,用观察法配平,二氧化碳后面标上上升符号;
(3)A与D反应得到的气体产物是二氧化碳,二氧化碳的检验方法是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳,反应物是二氧化碳和氢氧化钙,生成物是碳酸钙和水,碳酸钙后面标上沉淀符号.
故答案为:(1)有气泡产生,溶液由无色变为浅绿色;(2)Fe+2HCl═FeCl2+H2↑;置换反应;Na2CO3+2HCl═2NaCl+H2O+CO2↑;(3)澄清石灰水;Ca(OH)2+CO2═CaCO3↓+H2O.
(1)铁与盐酸反应生成氯化亚铁和氢气,亚铁离子溶液是浅绿色,所以反应现象是:有气泡产生,溶液由无色变为浅绿色;
(2)A与C反应的反应物是铁和盐酸,生成物是氯化亚铁和氢气,用观察法配平,氢气后面标上上升符号;反应物中有一种是单质,有一种是化合物,生成物中有一种是单质,有一种是化合物,所以反应类型是置换反应;A与D反应的反应物是碳酸钠和盐酸,生成物是氯化钠、水和二氧化碳,用观察法配平,二氧化碳后面标上上升符号;
(3)A与D反应得到的气体产物是二氧化碳,二氧化碳的检验方法是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳,反应物是二氧化碳和氢氧化钙,生成物是碳酸钙和水,碳酸钙后面标上沉淀符号.
故答案为:(1)有气泡产生,溶液由无色变为浅绿色;(2)Fe+2HCl═FeCl2+H2↑;置换反应;Na2CO3+2HCl═2NaCl+H2O+CO2↑;(3)澄清石灰水;Ca(OH)2+CO2═CaCO3↓+H2O.
点评:解答本题关键是要利用酸的化学性质:酸能与金属反应,酸能与碱反应,酸能与盐反应,这是解决该题的关键.再利用各反应的生成物,推出实验现象,再进一步进行分析.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
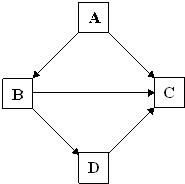 物质之间的相互转化是化学中的重要知识.某同学在复习物质性质时,绘制了框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.
物质之间的相互转化是化学中的重要知识.某同学在复习物质性质时,绘制了框图.框图中“→”表示物质之间可以向箭头所指方向一步转化.根据框图,回答下列问题.
 A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现用MgSO4 溶液按右图所示的操作,可将它们
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现用MgSO4 溶液按右图所示的操作,可将它们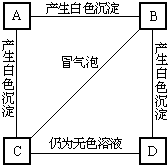 (1)A、B、C、D分别是Ba(NO3)2、Na2CO3、MgCl2和H2SO4中的各一种溶液.从表标明了它们之间两两相混的现象:根据实验事实可知:
(1)A、B、C、D分别是Ba(NO3)2、Na2CO3、MgCl2和H2SO4中的各一种溶液.从表标明了它们之间两两相混的现象:根据实验事实可知: