题目内容
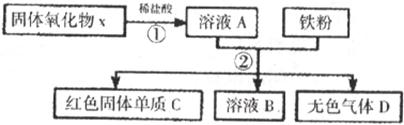
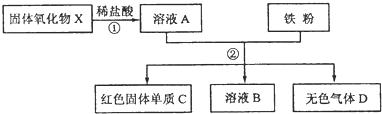
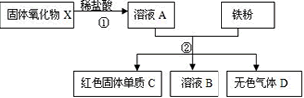
某固体氧化物X,经过①②两步反应后,得到红色固体单质C,溶液B只含一种溶质,且是盐.反应物和产物均已给出.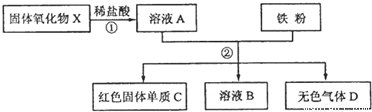
(1)第①步盐酸是否过量? ,判断根据是 .
(2)写出①中发生反应的化学方程式: .
(3)写出生成C的化学方程式: .
【答案】分析:可以根据物质的性质和物质之间相互作用的实验现象等方面进行分析、解答.例如,铜是红色物质,稀盐酸和铁反应生成无色的氢气.
解答:解:氧化铜和稀盐酸反应生成氯化铜和水,氯化铜和铁反应生成氯化亚铁和铜,稀盐酸和铁反应生成氯化亚铁和氢气.
故填:(1)是;如第一步盐酸不过量,第二步就不会产生气体.
(2)CuO+2HCl=CuCl2+H2O
(3)Fe+CuCl2=FeCl2+Cu
点评:本题主要考查了如何根据物质的性质判断物质的组成及其正确书写化学方程式的问题.
解答:解:氧化铜和稀盐酸反应生成氯化铜和水,氯化铜和铁反应生成氯化亚铁和铜,稀盐酸和铁反应生成氯化亚铁和氢气.
故填:(1)是;如第一步盐酸不过量,第二步就不会产生气体.
(2)CuO+2HCl=CuCl2+H2O
(3)Fe+CuCl2=FeCl2+Cu
点评:本题主要考查了如何根据物质的性质判断物质的组成及其正确书写化学方程式的问题.

练习册系列答案
相关题目