题目内容
人类生产和生活中都离不开金属。
(1)用铜丝作导线,主要利用其延展性和______性。
(2)铁生锈的条件是 。
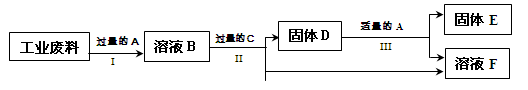
(3)某工厂废料中可能含有铜、氧化铜和碳粉中的一种或几种。为确定其成分,设计如下流程并实验。
【资料:CuO + H2SO4 = CuSO4 + H2O】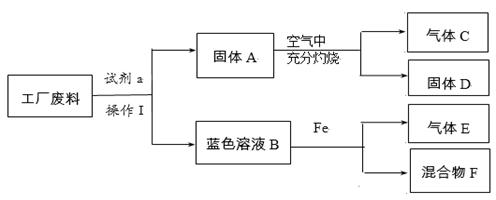
根据流程回答下列问题:
①实验操作Ⅰ的名称是______。
②蓝色溶液B与Fe反应的化学方程式是 。
③废料的成分是
(1)导电(2)与氧气和水同时接触(3)①过滤②Fe + H2SO4 = FeSO4 + H2↑ Fe + CuSO4 = FeSO4 + Cu (各1分)③铜、氧化铜和碳粉
解析试题分析:(1)用铜丝作导线,主要利用其延展性和导电性;(2)铁生锈的条件是与氧气和水同时接触;(3)因为操作后固液分离,故①实验操作Ⅰ的名称是过滤;②蓝色溶液B中含有硫酸和硫酸铜故与Fe反应的化学方程式是Fe + H2SO4 = FeSO4 + H2↑,Fe + CuSO4 = FeSO4 + Cu,③废料的成分是为铜、氧化铜和碳粉
考点:金属材料、物质成分的推断

(7分)人类的生产、生活离不开金属。
(1)地壳中含量最高的金属元素是 。
(2)用铜制电线主要是利用铜具有良好的延展性和 性。
(3)将生锈的铁片放入足量稀硫酸中,发生置换反应的化学方程式为 。
(4)在硫酸铜和硫酸亚铁的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中滴加稀硫酸,无气泡产生。则滤渣中的金属是 ,滤液中溶质的组成是 (写出所有可能)。
(5)将质量相等的锌粉和铁粉,分别放入两个烧杯中,再分别倒入质量相等、溶质的质
量分数相同的稀盐酸,充分反应,生成氢气的质量(m)随反应时间(t)变化的曲
线如图所示。下列说法正确的是 (填字母序号)。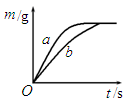
| A.消耗两种金属的质量相等 |
| B.两烧杯中金属都没有剩余 |
| C.两烧杯中稀盐酸都没有剩余 |
| D.曲线a表示锌和稀盐酸的反应 |
铬(Cr)是一种重要的金属材料,它具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬、锰、镍组成合金可以制成各种性能的不锈钢。某校化学研究小组对Cr(铬)、Al、Cu的金属的活动性顺序进行探究,过程如下:
(1)[作出假设]对三种金属的活动性顺序提出三种可能的假设是:
①Cr>Al>Cu②Al>Cr>Cu③Cr>Cu>Al
[设计实验]同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象,记录以下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应现 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
[控制实验条件]三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是 。
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使金属温度相同,易反应
[得出结论]原假设中正确的是 (选填假设中①、②,③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式 。
[结论应用]根据探究结果,请你预测铬与硫酸铜溶液 (填“能”或“不能”)反应,理由是 。