题目内容
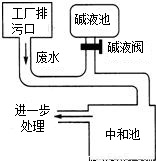
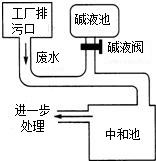 右图为硫酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱中和.工业生产中,在测定废水(假设只含硫酸)中硫酸的质量分数的基础上,通过调节碱液阀控制碱液的流量(单位时间排出碱液的量)达到中和废水的目的.
右图为硫酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱中和.工业生产中,在测定废水(假设只含硫酸)中硫酸的质量分数的基础上,通过调节碱液阀控制碱液的流量(单位时间排出碱液的量)达到中和废水的目的.
已知:中和50 mL废水需要l%NaOH溶液40 mL.试求:
废水中硫酸的质量分数.(假设废水和NaOH溶液的密度均为1 g?cm-3)
解:设废水中硫酸的质量分数为x.
2NaOH+H2SO4=Na2SO4↓+2H2O
80 98
40mL×1g?cm-3×1% 50mL×1g?cm-3×x
 =
=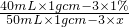
x=0.98%
答:废水中硫酸的质量分数是0.98%.
分析:氢氧化钠与硫酸反应生成盐和水,我们利用氢氧化钠可以中和废水中的硫酸.我们在计算时应先将体积转化为质量再进行计算.
点评:在计算废水中硫酸的质量分数时,先将溶液的体积转化为质量,然后再进行计算.
2NaOH+H2SO4=Na2SO4↓+2H2O
80 98
40mL×1g?cm-3×1% 50mL×1g?cm-3×x
 =
=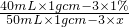
x=0.98%
答:废水中硫酸的质量分数是0.98%.
分析:氢氧化钠与硫酸反应生成盐和水,我们利用氢氧化钠可以中和废水中的硫酸.我们在计算时应先将体积转化为质量再进行计算.
点评:在计算废水中硫酸的质量分数时,先将溶液的体积转化为质量,然后再进行计算.

练习册系列答案
相关题目
下表为氯化钠、硝酸钾和氢氧化钙在不同温度下的溶解度.
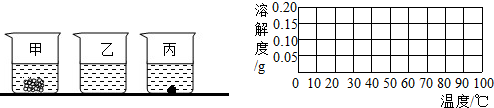
(1)20℃时分别往盛有100g水的烧杯中加入上述三种物质各35g,充分溶解后如右图所示,则乙烧杯中的溶质是 .
(2)要使丙烧杯中的固体完全溶解,可采取的一种措施是 .
(3)请根据上表数据在右图表格中画出氢氧化钙的溶解度曲线.
(4)熟石灰常用作中和硫酸厂排放的少量硫酸现有100t含硫酸0.49%的废水,该废水含有硫酸的质量 ,完全处理这些废水需要氢氧化钙的质量是 .
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶 解/g 度 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| Ca(OH)2 | 0.187 | 0.178 | 0.165 | 0.153 | 0.141 | 0.129 | 0.116 | |
(2)要使丙烧杯中的固体完全溶解,可采取的一种措施是
(3)请根据上表数据在右图表格中画出氢氧化钙的溶解度曲线.
(4)熟石灰常用作中和硫酸厂排放的少量硫酸现有100t含硫酸0.49%的废水,该废水含有硫酸的质量

(2011?增城市一模)下表为氯化钠、硝酸钾和氢氧化钙在不同温度下的溶解度.
(1)20℃时分别往盛有100g水的烧杯中加入上述三种物质各35g,充分溶解后如右图所示,则乙烧杯中的溶质是.
(2)要使丙烧杯中的固体完全溶解,可采取的一种措施是.
(3)请根据上表数据在右图表格中画出氢氧化钙的溶解度曲线.
(4)熟石灰常用作中和硫酸厂排放的少量硫酸现有100t含硫酸0.49%的废水,该废水含有硫酸的质量,完全处理这些废水需要氢氧化钙的质量是.

| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | ||
| 溶 解/g 度 | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| Ca(OH)2 | 0.187 | 0.178 | 0.165 | 0.153 | 0.141 | 0.129 | 0.116 | |
(2)要使丙烧杯中的固体完全溶解,可采取的一种措施是.
(3)请根据上表数据在右图表格中画出氢氧化钙的溶解度曲线.
(4)熟石灰常用作中和硫酸厂排放的少量硫酸现有100t含硫酸0.49%的废水,该废水含有硫酸的质量,完全处理这些废水需要氢氧化钙的质量是.

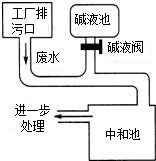 右图为硫酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱中和.工业生产中,在测定废水(假设只含硫酸)中硫酸的质量分数的基础上,通过调节碱液阀控制碱液的流量(单位时间排出碱液的量)达到中和废水的目的.
右图为硫酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱中和.工业生产中,在测定废水(假设只含硫酸)中硫酸的质量分数的基础上,通过调节碱液阀控制碱液的流量(单位时间排出碱液的量)达到中和废水的目的.