题目内容
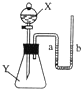 如图所示,锥形瓶内盛有物质Y,分液漏斗内盛有液体X,U型管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时,请你回答下列问题:
如图所示,锥形瓶内盛有物质Y,分液漏斗内盛有液体X,U型管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时,请你回答下列问题:(1)若X为氢氧化钠溶液,Y为二氧化碳气体,则U形管内a液面
高于
高于
b液面(填“高于”、“低于”或“等于”,下同).写出反应的化学方程式CO2+2NaOH=Na2CO3+2 H2O
CO2+2NaOH=Na2CO3+2 H2O
.(2)若X为稀盐酸,Y为大理石,则U型管内a液面
低于
低于
b液面.你的理由是二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面
二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面
.分析:(1)二氧化碳能够被氢氧化钠溶液吸收,会使瓶内压强发生变化;
根据反应物和生成物,正确书写化学方程式;
(2)稀盐酸与大理石反应,生成二氧化碳气体,引起瓶内气体压强明显上升.
根据反应物和生成物,正确书写化学方程式;
(2)稀盐酸与大理石反应,生成二氧化碳气体,引起瓶内气体压强明显上升.
解答:解:(1)氢氧化钠溶液能够吸收二氧化碳气体,从而使得锥形瓶内的压强减小.故填:高于.
氢氧化钠和二氧化碳反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
(2)稀盐酸与大理石反应,生成二氧化碳气体,引起瓶内气体压强明显上升.则U型管内a液面 低于b液面.你的理由是 二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面
故答案为:(1)高于; CO2+2NaOH=Na2CO3+2 H2O;
(2)低于; 二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面.
氢氧化钠和二氧化碳反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
(2)稀盐酸与大理石反应,生成二氧化碳气体,引起瓶内气体压强明显上升.则U型管内a液面 低于b液面.你的理由是 二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面
故答案为:(1)高于; CO2+2NaOH=Na2CO3+2 H2O;
(2)低于; 二者反应产生气体,瓶内气体压强明显上升,气体通过玻管压入使a液面低于b液面.
点评:解答本题要掌握化学方程式的书写方法和各种物质的性质等方面的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
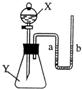 25、如图所示,锥形瓶内盛有物质Y,分液漏斗内盛有液体X,U型管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴人锥形瓶内时,请你回答下列问题:
25、如图所示,锥形瓶内盛有物质Y,分液漏斗内盛有液体X,U型管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴人锥形瓶内时,请你回答下列问题: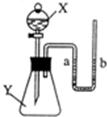
 9、如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
9、如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )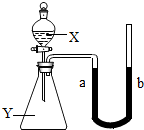 (2005?包头)如图所示,锥形瓶内盛有物质Y(可能为气体、溶液或固体),分液漏斗内盛有液体X,U形管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时.回答下列问题:
(2005?包头)如图所示,锥形瓶内盛有物质Y(可能为气体、溶液或固体),分液漏斗内盛有液体X,U形管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时.回答下列问题: