题目内容
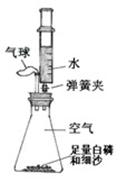
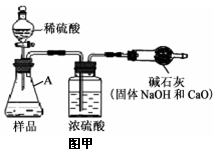
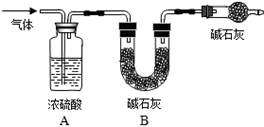
小燕同学在实验室发现一瓶标签破损的无色液体(如图),她根据目前所学的知识,大胆猜想并设计实验进行验证,请你参与她的探究。

提出假设:该无色液体可能是______或___________

提出假设:该无色液体可能是______或___________

H2O,H2O2(双氧水)(或硫酸溶液)


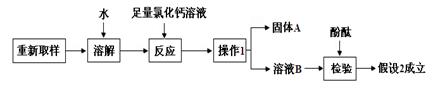
根据化学式的特点,H元素在前的化合物常见的为氧化物和酸,所以,符合组成特点的物质有:水(H2O)、过氧化氢(H2O2)、硫酸(H2SO4)、碳酸(H2CO3),其中碳酸因不稳定,实验室没有碳酸溶液。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目