题目内容
【题目】根据下列所给实验室常用制气装置回答问题。

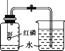
(1)B装置中一处明显的错误是____________________,利用改正后的装置完成后面的实验;
(2)实验室加热二氧化锰和氯酸钾固体混合物制取氧气,若需收集一瓶较纯净的氧气,则其发生和收集装置应选择_________________,发生反应的化学方程式为___________其中MnO2起_____________________作用;
(3)若用稀盐酸与石灰石制取二氧化碳,应选用的发生和收集装置是____________________;实验中判断二氧化碳是否收集满的操作方法是____________________;反应产生的二氧化碳在收集之前,需将气体先通过F装置进行除杂,则该装置中加入的药品需更换为____________________。
(4)已知氯气(Cl2)在常温常压下为黄绿色有刺激性气味的有毒气体,易溶于水,密度比空气大,若用G装置收集氯气,气体应该从__________________________(填“a”或“b”)端通入。
【答案】长颈漏斗下端未伸入液面以下 AC 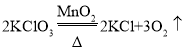 催化 BE 将燃着的木条放在 E装置的集气瓶瓶口,若木条立即熄灭,说明二氧化碳已经收集满 饱和碳酸氢钠溶液 a
催化 BE 将燃着的木条放在 E装置的集气瓶瓶口,若木条立即熄灭,说明二氧化碳已经收集满 饱和碳酸氢钠溶液 a
【解析】
(1)装置B中长颈漏斗下端必须伸入液面以下,形成液封,防止气体从长颈漏斗的上端口逸出;
(2)由于氯酸钾和二氧化锰均为固体,且反应需要在加热条件下进行,所以发生装置选择A,由于氧气的密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,但用排水法收集的气体相对比较纯净,故可选用C装置收集氧气,故发生装置和收集装置应选择AC;
用氯酸钾制取氧气的反应原理是氯酸钾在二氧化锰的催化作用下加热分解反应生成氯化钾和氧气,其化学反应方程式为: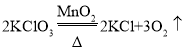 ;
;
其中二氧化锰可加快氯酸钾的分解,起催化作用;
(3)用稀盐酸与石灰石制取CO2时,发生装置为固液常温型,发生装置应选B,CO2能溶于水且与水反应,密度大于空气,应用向上排空气法收集,收集装置应选E,故发生和收集装置应选BE;
二氧化碳验满时,将燃着的木条放在集气瓶瓶口,若木条立即熄灭,证明二氧化碳气体已集满;
用稀盐酸与石灰石反应制取CO2时,二氧化碳中常混有HCl杂质,所以装置中的药品需更换为饱和碳酸氢钠溶液;
(4)由于氯气易溶于水且密度比空气大,所以气体从G装置的a端通入。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验设计 |
|
|
|
|
实验目的 | 探究二氧化锰能否加快过氧化氢分解 | 探究石蜡燃烧后是否有二氧化碳生成 | 检验氧气是否集满 | 测定空气中氧气的含量 |
A. A B. B C. C D. D
【题目】阅读下面科普短文。
“菠菜豆腐”是我国的传统菜肴,近年来,有关“菠菜豆腐”的争论主要集中在钙吸收率方面。菠菜中富含易溶于水的草酸,若单独吃菠菜,其中的草酸会结合胃内食糜中的部分铁和锌,还能够进入血液,沉淀血液中所含的钙。而将豆腐与菠菜同食,豆腐中的可溶性钙与菠菜中的草酸结合成不溶性的草酸钙(CaC2O4)沉淀,既能够保护食物中的铁和锌等元素,还能保证人体内的钙不被草酸结合。因此,豆腐与菠菜同食仍不失为一个好的搭配。
研究人员以新鲜菠菜和新鲜豆腐为材料,进行了“菠菜豆腐”烹调方法的研究。
(实验1)探究菠菜质量对菜肴中可溶性钙含量的影响。实验结果如下:
豆腐/ g | 10 | 10 | 10 | 10 | 10 |
菠菜/ g | 5 | 10 | 15 | 20 | 25 |
可溶性钙/总钙 | 0.364 | 0.287 | 0.186 | 0.125 | 0.088 |
(实验2)探究菠菜焯水时间对菜肴中可溶性钙含量的影响。
用100g豆腐和250g菠菜(焯水时间不同)制成菜肴,测定每100g“菠菜豆腐”中可溶性钙的质量,结果见下图。

以上研究表明,烹调“菠菜豆腐”时,如能适当减少菠菜的比例,并预先将菠菜焯水,则豆腐中钙的吸收率将会显著提高。
根据文章内容,回答下列问题:
(1)可溶性钙中的“钙”是指_________(“钙单质”或“钙元素”)。
(2)豆腐中富含的营养素是_____________。
A. 维生素 B. 糖类 C. 蛋白质 D. 油脂
(3)结合实验1的数据分析,可得到的结论是_________________。
(4)用焯水后的菠菜制作“菠菜豆腐”,能提高可溶性钙含量的原因是__________。
(5)草酸钙在高温下完全分解可得到两种气态氧化物和一种固态氧化物,该反应的化学方程式为____________________。