题目内容
为了弘扬中华民族的传统文化,某校在端午节开展了包粽子活动.
(1)老师准备了糯米、鲜猪肉、植物油、调味品等原谅以及粽叶,在各种原料中富含糖类的是 .
(2)粽子吃起来咸淡适中,有同学猜想其中一定含有食盐.于是从煮过粽子的锅里取少量的水于试管中,滴加硝酸银溶液,产生了不溶于稀硝酸的白色沉淀,你认为这样的实验现象能否证明食盐的存在,并说明理由. .
(1)糯米;(2)不能,本实验只能证明氯离子的存在.
解析

 名校课堂系列答案
名校课堂系列答案在生活中经常曝出某品牌金饰品掺假的事件,引起学生的好奇,某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】
(1)假黄金通常是黄铜(Cu﹣Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】
(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是 (填名称),说明此样品为 (填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银 |
| 把铂浸入氯化钯溶液中 | | 钯的活动性比铂强 |
【废液处理】
(1)转化成沉淀.小组同学所有液体倒入废液缺缸中,出现白色沉淀.写出产生该现象的化学方程式: (写出一个即可).
(2)通过科学合理的方法进一步回收金属钯.
早在春秋战国时期,我国就开始生产和使用铁器。
(1)写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式 ,盛水的铁锅与水面接触的一圈最易生锈,钢铁生锈的条件是 ,利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的 (填字母)。
| A.耐腐蚀性 | B.延展性 | C.导热性 | D.导电性 |
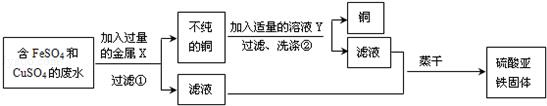
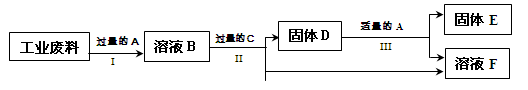
金属X是 ,写出上述实验方案中有关反应的化学方程式
① ;② 。
(12分)碱式碳酸盐广泛应用于工农业生产。
(1)某碱式碳酸盐样品M(OH)2·MCO3,为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响)。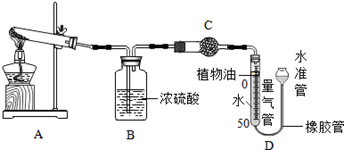
①连接装置并 ;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④加热至样品质量不再减少;⑤冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算。
Ⅰ.请将上述实验步骤补充完整;
Ⅱ.装置B的作用是 ,少量植物油的作用是 ,C中的试剂是 (填字母序号);
a.碱石灰 b.浓硫酸 c.硫酸铜
Ⅲ.步骤⑥中调节液面相平的操作是将水准管 (填“缓慢上移”或“缓慢下移”)。
Ⅳ.若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是 (填字母序号);
a.反应前量气管水面在0刻度处,反应后仰视读数
b.样品未分解完全即停止实验
c.量气管中未加植物油
(2)实际生产中的碱式碳酸铜可表示为Cu(OH)2·mCuCO3,某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示。取3组数据的值得到CO2的体积为 mL,又知常温常压下CO2的密度为1.964 g/L,据此计算m的值。(写出计算m的过程,最后结果保留小数点后两位) 。
| 组别 | 样品质量 | CO2体积 |
| 第1组 | 0.21 g | 22.39 mL |
| 第2组 | 0.21 g | 22.41 mL |
| 第3组 | 0.21 g | 22.40 mL |