题目内容
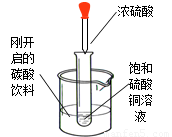
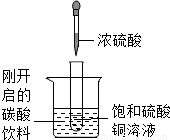
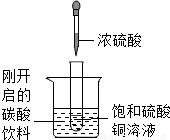
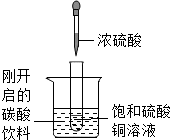 如图所示,把试管小心放入盛有(20℃)碳酸饮料的烧杯中,试管中先放入适量饱和硫酸铜溶液,再用滴管滴加5ml浓硫酸于试管中,试回答下列问题:
如图所示,把试管小心放入盛有(20℃)碳酸饮料的烧杯中,试管中先放入适量饱和硫酸铜溶液,再用滴管滴加5ml浓硫酸于试管中,试回答下列问题:
(1)实验中可观察到的现象是
①______,
②______,烧杯中现象产生的原因是______.
(2)实验中表现出浓硫酸的______性,烧杯中所发生反应的化学方程式为______.
解:(1)由于浓硫酸具有吸水性,当把浓硫酸加入硫酸铜溶液中时,会吸收溶液中的水,使饱和硫酸铜溶液中的水减少,导致溶液中有晶体的析出;又因为浓硫酸溶于水会放出大量的热,使烧杯中碳酸饮料的温度升高,碳酸分解产生二氧化碳,而产生大量的气泡;
(2)硫酸铜溶液中析出晶体说明了浓硫酸的吸水性,根据化学方程式的书写步骤,方程式为:H2CO3 H2O+CO2↑.
H2O+CO2↑.
故答案为:(1)①小试管中有晶体析出②烧杯中产生大量气泡;由于浓硫酸溶于硫酸铜溶液,放出大量的热,致使烧杯中饮料温度升高,碳酸分解产生二氧化碳;
(2)吸水性;H2CO3 H2O+CO2↑
H2O+CO2↑
分析:(1)根据饱和溶液和不饱和溶液的相互转化的方法解答;
(2)根据浓硫酸及碳酸的性质回答.
点评:熟练运用饱和溶液与不饱和溶液的相互转化方法,及浓硫酸的特性和碳酸的不稳定性是解决本题的关键.
(2)硫酸铜溶液中析出晶体说明了浓硫酸的吸水性,根据化学方程式的书写步骤,方程式为:H2CO3
 H2O+CO2↑.
H2O+CO2↑.故答案为:(1)①小试管中有晶体析出②烧杯中产生大量气泡;由于浓硫酸溶于硫酸铜溶液,放出大量的热,致使烧杯中饮料温度升高,碳酸分解产生二氧化碳;
(2)吸水性;H2CO3
 H2O+CO2↑
H2O+CO2↑分析:(1)根据饱和溶液和不饱和溶液的相互转化的方法解答;
(2)根据浓硫酸及碳酸的性质回答.
点评:熟练运用饱和溶液与不饱和溶液的相互转化方法,及浓硫酸的特性和碳酸的不稳定性是解决本题的关键.

练习册系列答案
相关题目
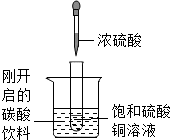 如图所示,把试管小心放入盛有(20℃)碳酸饮料的烧杯中,试管中先放入适量饱和硫酸铜溶液,再用滴管滴加5ml浓硫酸于试管中,试回答下列问题:
如图所示,把试管小心放入盛有(20℃)碳酸饮料的烧杯中,试管中先放入适量饱和硫酸铜溶液,再用滴管滴加5ml浓硫酸于试管中,试回答下列问题: