题目内容
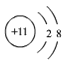
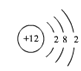
【题目】A—H都是初中化学常见物质。其中A、B的组成元素相同,且常温下都是无色液体;H是蓝色沉淀。X、Y都是氧化物,其中X是黑色粉末固体,Y常用作食品干燥剂,Z是红色固体。他们之间有如下转化关系。
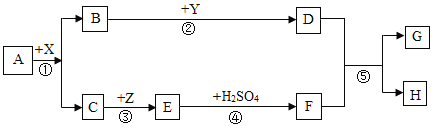
根据上述信息,回答下列问题:
⑴E的化学式是_____。
⑵应②的化学方程式_____。
⑶应⑤的化学方程式_____。此反应的基本反应类型是_____反应。
【答案】CuO CaO+H2O=Ca(OH)2 CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4 复分解
【解析】
(1)A-H都是初中化学常见物质,Y常用作食品干燥剂,所以Y是氧化钙,A、B的组成元素相同,且常温下都是无色液体,X是黑色粉末状固体,氧化钙会与B反应是B是水,A是过氧化氢溶液,过氧化氢分解生成水和氧气,所以C是氧气,X是二氧化锰,Z是红色固体,所以Z是铜,E是氧化铜,氧化铜和硫酸反应生成硫酸铜和水,所以F是硫酸铜,氧化钙和水反应生成氢氧化钙,所以D是氢氧化钙,氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,H是蓝色沉淀,所以H是氢氧化铜,G是硫酸钙,经过验证,推导正确,所以E的化学式是CuO;
(2)反应②是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(3)反应⑤是氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,化学方程式为:CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4,该反应属于复分解反应。
故答案为:(1)CuO;
(2)CaO+H2O=Ca(OH)2;
(3)CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4,复分解。

【题目】如图是模拟海水制盐的流程
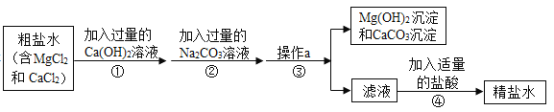
(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若_____________(填实验现象),则证明Ca(OH)2溶液已过量。
(2)实验结束后,兴趣小组对滤液进行探究
(提出问题)滤液中除了含有水和氯化钠外,还含有哪些溶质?
(提出猜想)根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的___________.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有___________和___________.
(验证猜想)
步骤 | 实验操作 | 实验现象 | 推断 |
1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | ___________ | 滤液中还含有___________溶质 |
2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入__________ | ___________ | 滤液中还含有氢氧化钠 |
(实验结论)经过兴趣小组的实验分析,推出猜想三是正确的.
(反思与拓展)为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:___________________________________________.
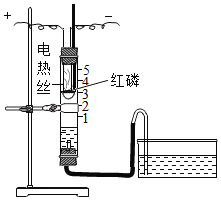
【题目】利用如图装置进行空气中氧气含量测定实验。
实验装置 | 实验操作 |
| I.向玻璃管和水槽内加适量的水,在燃烧匙里放足量红磷,塞紧塞子,上下移动水槽至两边水面相平于玻璃管的零刻度位置。 II.接通电源,待红磷燃烧,断开电源。 III.当温度恢复至室温,水不再进入玻璃管时,上下移动水槽至两边水面相平。 |
(1)实验中加入足量红磷的目的是_____,该实验中发生反应的化学方程式为_____。
(2)实验结束后,玻璃管内水面最终到达刻度线_____(填数字序号)处。
(3)实验操作I、III中,上下移动水槽至两边水面相平的目的是_____。