题目内容
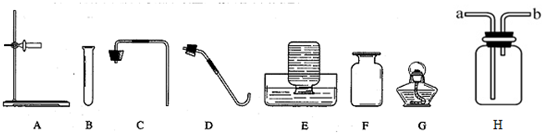
现有如图所示的实验装置:

(1)写出图中指定仪器的名称:①______ ②______
(2)写出用A装置制取氧气的化学方程式______.
(3)不同的装置有不同的优点,B、C都可以做制取气体的反应发生装置,说出B与C相比,B装置的优点是______;
如果用C装置制取气体,如果想使反应停止,应该采取的操作是______
(4)实验室现用锌粒与稀硫酸反应制取和收集一瓶干燥的氢气,应选用上述______组合.
(5)实验室制取氨气可用加热氯化铵与熟石灰两种固体来反应得到,已知氨气的密度比空气小,有刺激性气味(会污染空气),易溶于水,根据以上相关知识,你认为制取氨气应选用的发生装置是______,反应的化学方程式______;
(6)为了防止空气污染,要收集一瓶氨气最好选用以上装置______,气体从______端导入.
解:(1)酒精灯实验室常用的加热工具,长颈漏斗方便加液体药品,故答案为:酒精灯;长颈漏斗;
(2)制取装置包括加热和不需加热两种,如果用高锰酸钾或氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KClO3 2KCl+3O2↑或2KMnO4
2KCl+3O2↑或2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)B装置的优点是可以控制反应的速率,如果用C装置制取气体,如果想使反应停止,应该采取的操作是关闭止气夹b,故答案为:可以控制反应的速率;关闭止气夹b;
(4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集,故答案为:CE
(5)实验室制取氨气可用加热氯化铵与熟石灰两种固体来反应得到,因此需要加热;氯化铵与熟石灰反应生成氯化钙和水和氨气,配平即可,故答案为:A;2NH4Cl+Ca(OH)2 CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;
(6)为了防止空气污染,要收集一瓶氨气最好选用装置G,气体从长管a端导入,因为氨气的密度比空气小,故答案为:G;长管a;
分析:酒精灯实验室常用的加热工具,长颈漏斗方便加液体药品;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.B装置的优点是可以控制反应的速率,如果用C装置制取气体,如果想使反应停止,应该采取的操作是关闭止气夹b;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集.实验室制取氨气可用加热氯化铵与熟石灰两种固体来反应得到,因此需要加热;氯化铵与熟石灰在加热的条件下反应生成氯化钙和水和氨气,配平即可.为了防止空气污染,要收集一瓶氨气最好选用装置G,气体从长管a端导入,因为氨气的密度比空气小.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.
(2)制取装置包括加热和不需加热两种,如果用高锰酸钾或氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KClO3
 2KCl+3O2↑或2KMnO4
2KCl+3O2↑或2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;(3)B装置的优点是可以控制反应的速率,如果用C装置制取气体,如果想使反应停止,应该采取的操作是关闭止气夹b,故答案为:可以控制反应的速率;关闭止气夹b;
(4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集,故答案为:CE
(5)实验室制取氨气可用加热氯化铵与熟石灰两种固体来反应得到,因此需要加热;氯化铵与熟石灰反应生成氯化钙和水和氨气,配平即可,故答案为:A;2NH4Cl+Ca(OH)2
 CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑;(6)为了防止空气污染,要收集一瓶氨气最好选用装置G,气体从长管a端导入,因为氨气的密度比空气小,故答案为:G;长管a;
分析:酒精灯实验室常用的加热工具,长颈漏斗方便加液体药品;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.B装置的优点是可以控制反应的速率,如果用C装置制取气体,如果想使反应停止,应该采取的操作是关闭止气夹b;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集.实验室制取氨气可用加热氯化铵与熟石灰两种固体来反应得到,因此需要加热;氯化铵与熟石灰在加热的条件下反应生成氯化钙和水和氨气,配平即可.为了防止空气污染,要收集一瓶氨气最好选用装置G,气体从长管a端导入,因为氨气的密度比空气小.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
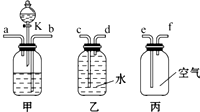 现有CO和CO2组成的混合气体,为了将它们分开,得到较纯净的CO和CO2,某中学课题研究小组设计了如图所示的实验装置(甲为分离装置,乙和丙为收集装置),其中所用的化学试剂可能为:①饱和石灰水;②稀硫酸;③稀盐酸.(CO的密度比空气略小,且难溶于水)
现有CO和CO2组成的混合气体,为了将它们分开,得到较纯净的CO和CO2,某中学课题研究小组设计了如图所示的实验装置(甲为分离装置,乙和丙为收集装置),其中所用的化学试剂可能为:①饱和石灰水;②稀硫酸;③稀盐酸.(CO的密度比空气略小,且难溶于水)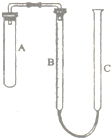 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
