题目内容
【题目】过氧乙酸(C2H4O3)广泛应用于环境的消毒,下列说法正确的是
A.过氧乙酸是由碳、氢、氧三种元素组成的
B.一个过氧乙酸分子是由2个碳元素和3个氧原子和4个氢原子构成
C.过氧乙酸中碳元素的质量分数是40%
D.过氧乙酸中碳、氢、氧元素的质量比为2:4:3
【答案】A
【解析】
A、根据过氧乙酸(C2H4O3)化学式可知,过氧乙酸是由碳、氢、氧三种元素组成的,故A正确;
B、根据过氧乙酸(C2H4O3)化学式可知,一个过氧乙酸分子是由2个碳原子和3个氧原子和4个氢原子构成,元素只讲种类,不论个数,故B错误;
C、过氧乙酸中碳元素的质量分数=![]() ≠40%,故C错误;
≠40%,故C错误;
D、过氧乙酸中碳、氢、氧元素的质量比=(12×2):(1×4):(16×3)≠2:4:3,故D错误。故选A。

【题目】某化学小组经查阅资料发现:镁除了能与氧气、盐酸、硫酸铜溶液反应,还能与饱和碳酸氢钠溶液反应。该组同学对镁的这种化学性质产生了兴趣,设计了如下实验方案进行探究:
活动一:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量的气泡和白色不溶物。
(1)收集并点燃产生的气体,火焰呈淡蓝色,火焰上方罩涂有澄清石灰水的小烧杯,无现象。则该气体为_____。
(2)同学们对白色不溶物做出如下猜测:
(猜想假设)①白色不溶物可能是Mg(OH)2;
②白色不溶物可能是MgCO3;
③白色不溶物可能是_____。活动二:设计定量实验确定白色不溶物成分。
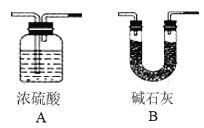
(查阅资料)①碱石灰主要成分是NaOH和CaO的混合物。
②MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
请写出MgCO3加热分解的化学方程式:_____。
(进行实验)
操作 | 现象 | 结论 |
①取反应结束洗净后的白色不溶物,加入足量的_____。 | 观察到_____ | 白色固体一定含有MgCO3 |
②称取一定量白色不溶物,充分加热至不再产生气体,将产生的气体先通入碱石灰,再通入浓硫酸,分别称量装置反应前后的质量 | _____ | 白色固体只含有MgCO3 |
(反思评价)同学们通过计算发现上述结论不正确,原因_____,他们通过讨论对上述实验又进行了改进,则该装置的正确连接顺序(装置可重复使用且每步反应均能完全进行):加热不溶物产生的气体→_____(填装置序号)