题目内容
【题目】铝是一种重要的金属,现实生活或生产中可谓“美铝如云”。
(1)铝原子的结构示意图为: 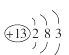 由此可知铝元素在元素周期表中位于第周期,在化学反应中易形成 离子(用化学符号表示)。
由此可知铝元素在元素周期表中位于第周期,在化学反应中易形成 离子(用化学符号表示)。
(2)将纯铝和铝合金(即硬铝)相互刻画,纯铝上留下明显划痕,这是因为铝用来制作高空电缆,说明铝具有性和性。根据表格中数据可知,用铝制作高空电览,这是因为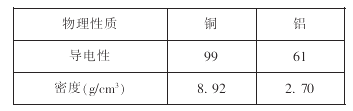
(3)人类在冶炼金属的历史进程中,下列金属距离现代最近的是
A.铜
B.铝
C.铁
(4)铝的化学性质很活泼,但家里用了很久的铝壶很少出现腐蚀,其中的原理是:。
(5)资料显示:铝与氢氧化钠和水反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;用112.5g含杂质4%的铝片(杂质对产生氢气的质量无影响)与足量的氢氧化钠和水充分反应,生成氢气的质量为克。
【答案】
(1)三,Al3+
(2)铝合金的硬度比纯铝大,导电性、延展性,铝的密度比铜小
(3)B
(4)铝与空气中的氧气发生反应生成一层致密的氧化膜,从而起了保护作用
(5)12
【解析】从图示看:铝元素在元素周期表中位于第三周期,在化学反应中易形成的离子是Al3+,将纯铝和铝合金(即硬铝)相互刻画,纯铝上留下明显划痕,这是因为铝用来制作高空电缆,说明铝具有导电性和延展性。根据表格中数据可知,用铝制作高空电览,这是因为铝的密度比铜小;人类在冶炼金属的历史进程中,金属距离现代最近的是铝,因为铝的好东西较强不容易炼制;铝的化学性质很活泼,但家里用了很久的铝壶很少出现腐蚀,其中的原理是:铝与空气中的氧气发生反应生成一层致密的氧化膜,从而起了保护作用。
设可以制取氢气的质量为X
2Al+2NaOH+2H2O=2NaAlO2+ | 3H2↑ |
54 | 6 |
112. 5g×(1-4%) | x |
列比例式得:54:112. 5g(1-4%)=6:X
解得:X=12g。
【考点精析】掌握金属的物理性质及用途和金属材料的选择依据是解答本题的根本,需要知道金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性;黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属.

【题目】豆腐是生活特别喜爱的食物。下表是豆腐中主要成分的平均质量分数:
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素B1 | 维生素B2 |
质量分数/% | 89.3 | 4.7 | 1.3 | 2.8 | 0.24 | 0.064 | 1.4 | 0.00006 | 0.00003 |
(1)在人体中,构成血红蛋白成分所需的微量元素是_____。
(2)蛋白质在人体中的主要作用是_____。