题目内容
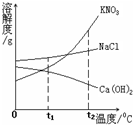 20、右图是KNO3、NaCl、Ca(OH)2三种物质的溶解度曲线图.请回答下列问题:
20、右图是KNO3、NaCl、Ca(OH)2三种物质的溶解度曲线图.请回答下列问题:(1)当温度在
t1~t2℃
范围中,KNO3与NaCl的溶解度相等.(2)当t1℃时的KNO3饱和溶液升温到t2℃时,KNO3溶液的溶质质量分数
不变
(填“变大”、“不变”或“变小”,下同)
(3)在t1℃时的饱和石灰水中加入少量CaO后恢复到t1℃时,溶液质量
变小
.分析:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②判断物质的溶解度随温度变化的变化情况,从而可以确定出温度变化时溶液中溶质质量分数的变化等.
解答:解:(1)根据两物质的溶解度曲线不难看出,两物质的溶解度曲线的交点所处的温度在t1℃和t2℃之间,故答案为:t1~t2℃
(2)由于硝酸钾的溶解度随温度的升高而增大,因此升温时它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,故答案为:不变
(3)饱和石灰水中的溶质是氢氧化钙,由于向石灰水中加入少量的生石灰时,生石灰就会和水发生反应生成氢氧化钙从而会使饱和溶液失去一部分水,原来溶解在这一部分水中的溶质也会结晶析出,因此溶液的质量会减小,故答案为:减小
(2)由于硝酸钾的溶解度随温度的升高而增大,因此升温时它的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,故答案为:不变
(3)饱和石灰水中的溶质是氢氧化钙,由于向石灰水中加入少量的生石灰时,生石灰就会和水发生反应生成氢氧化钙从而会使饱和溶液失去一部分水,原来溶解在这一部分水中的溶质也会结晶析出,因此溶液的质量会减小,故答案为:减小
点评:本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
 (2006?佛山)右图是KNO3和NaCl在水中的溶解度曲线.
(2006?佛山)右图是KNO3和NaCl在水中的溶解度曲线.
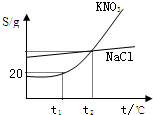 11、右图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
11、右图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( ) 右图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
右图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )