��Ŀ����
����Ŀ����7+4�֣���ѧ���о����ʵ���ɡ��ṹ�����ʼ��仯���ɵĿ�ѧ��
��1����ͭ�����ɱ������Ȼ������������У������ӹ��ɵ��� ����д��ţ���ͬ�����������˹�������� ��
��2��ʳ���к��д��ᣨCH3COOH���������� ��Ԫ����ɣ���������⡢��ԭ�Ӹ�����Ϊ ��
��3������A������B�Ӵ��ɷ�����Ӧ�����ɹ���C��Һ��D�����۹���������ʾ��
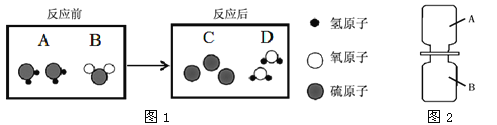
���÷�Ӧ�����У�������������� �������ƣ���
�������������ֻ����ƿ�зֱ�ʢ��A��B����ͼ2��ʾ����ʵ�顣��֪��ͬ�����£����������ȵ��ڷ��Ӹ����ȣ����ַ�Ӧ��ʣ��������� ���ѧʽ����
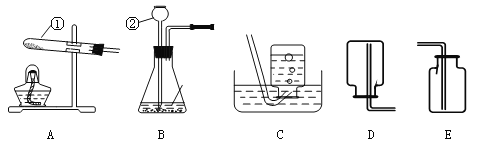
��4����ֽ�����������NaOH�ļ��Է�ˮ���辭���������Ժ��ŷš�
����pH��ֽ����ˮ�ʼ��ԣ���pH 7��
����ij��ֽ����ˮ�к�NaOH����������Ϊl.6%�����з�����9.8t��H2SO4����������Ϊ20%�������Դ����ķ�ˮ�����Ƕ��٣���д��������̣�
���𰸡���1���� �� ��2��3 2:1
��3������������ˮ(��д�����֣���д1����1�֣� �� SO2
��4���� >
��������
�����������1��ͭ����ͭԭ�ӹ��ɵģ�������̼���ɶ�����̼���ӹ��ɵģ��Ȼ������������Ӻ������ӹ��ɵģ��ɱ�����ʱҪ���մ������ȣ��ʿ������˹����ꣻ
��2���ɴ���Ļ�ѧʽ��֪����������̼���⡢������Ԫ����ɵģ������������ԭ�Ӻ���ԭ�ӵĸ�����Ϊ2:1��
��3�����ݷ�Ӧ����ʾ��ͼ��֪�÷�Ӧ�ķ�Ӧ��������Ͷ������������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�2H2S+SO2===3S+2H2O����������������Ԫ����ɵĻ��������һ����������ʶ��������ˮ�����������Ͷ�������Ӧʱ�ķ��Ӹ�����Ϊ2:1����������������ȣ���ô����������ʣ�ࣻ
��4���ټ�����Һ��PH����7��
���������������ᷴӦ���ɵ��������ƺ�ˮ�����û�ѧ�Ļ�ѧ����ʽ�������������������ᷴӦ�������ȼ��ɼ�����������Ƶ�������
�⣺����Դ����ķ�ˮ������Ϊx
2NaOH + H2SO4 = Na2SO4 + 2H2O
80 98
1.6%x 9.8t��20%
![]()
x=100t
�������Դ����ķ�ˮ������Ϊ 100t