题目内容
【题目】盐中含有金属离子(或铵根离子)和酸根离子,组成相似的盐具有一些相似的化学性质。
(1)向Cu(NO3)2溶液中加入NaOH溶液,充分振荡,反应的化学方程式为_____
(2)在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有______(任举一例);
(3)向CuSO4溶液中加入某种纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为_______
【答案】2NaOH+Cu(NO3)2=2NaNO3+Cu(OH)2↓ Ba(NO3)2或BaCl2等 Ba(OH)2
【解析】
(1)Cu(NO3)2溶液与NaOH溶液反应生成氢氧化铜沉淀和硝酸钠,反应的化学方程式为![]() 。
。
(2)硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜。在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有Ba(NO3)2或BaCl2等。
(3)硫酸铜和氢氧化钡反应生成硫酸钡和氢氧化铜沉淀。向CuSO4溶液中加入某种纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物为氢氧化钡,化学式为Ba(OH)2。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与探究并回答问题。
(提出猜想)假设l:红色粉末是铜粉; 假设2:红色粉末是氧化铁粉; 假设3:红色粉末是____。
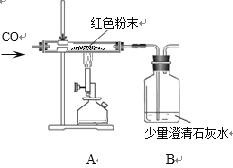
(实验探究)某同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按下图装置在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 | |
Ⅰ组 | 玻璃管和红色粉末的总质量为37.3 g | 玻璃管和固体物质的总质量为36.1 g |
Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0 g | 洗气瓶和瓶中物质的总质量为183.1 g |
(交流讨论)
(1)应该选择___________组的实验数据来计算确定组成.最终计算结果表明:该红色粉末的组成是假设____(填序号)成立。
(2)写出A装置中发生反应的化学方程式________________________;实验中观察到A装置中的现象为____________________。
(3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?请判断并说明理由:________________________________。
(反思评价)
(1)从环保角度,该装置有严重不足之处。你认为应该如何改进?____________________。
(2)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是_________________________。
(3)工业上用2000t含氧化铁75%的赤铁矿,可炼出含铁97%的生铁_________________吨?(结果保留一位小数)