题目内容
【题目】联合国大会宣布2019年是“国际化学元素周期表年”(IYPT2019)。下图中①是钙元素在元素周期表中的信息,A、B、C、D、E是某五种微粒的结构示意图。请回答下列问题:

(1)根据周期表信息,钙元素的相对原子质量为_____;
(2)在A、B、D、E微粒中,属于离子的是_____(填离子符号);化学性质相似的微粒是_____(填字母)。
(3)B微粒对应的元素位于元素周期表中第_____周期;若C微粒表示的是离子,则X为_____;E微粒在化学变化中容易_____电子(填“失去”或“得到”)。
【答案】40.08 Ca2+ A和B 三 8 失去
【解析】
(1)根据周期表信息,钙元素的相对原子质量为40.08;
(2)质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;在A、B、D、E微粒中,D的质子数>核外电子数,为阳离子,质子数是20,为钙离子,符号为:Ca2+;化学性质相似的微粒的是AB,这是因为它们的最外层电子数相等。
(3)B微粒对应的元素是硫,原子核外电子层数是3,位于元素周期表的第三周期;C的质子数是17,为氯元素,氯原子最外层电子数是7,大于4,易得到一个电子成为带一个负电荷的氯离子, 所以若C微粒表示的是离子,则X为8;E微粒最外层电子数为2,小于4,易失去2个电子。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。
实验装置 | 实验步骤及现象 |
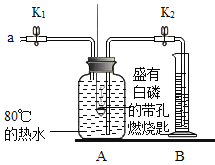
| 步骤1:检验装置的气密性,气密性良好 步骤2:将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧。 步骤3:向A瓶中加满80°C热水,塞紧瓶塞,白磷不燃烧。 步骤4:打开K1、K2,从A口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2,此时进入量筒B中水的体积为200mL ,观察到A瓶中的白磷燃烧。 |
[实验一](已知:白磷的着火点为40°C,白磷不溶于水也不与水反应)
(1)请写出白磷燃烧的化学方程式_________;
(2)对比步骤3和4的现象可知,可燃物燃烧的条件是________;
(3)待装置冷却--段时间后,打开K2如果观察到________;说明空气中氧气的体积约占1/5。
[实验二]

(1)按图实验(集气瓶底部有少量沙子)可观察到:镁条在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成。请写出反应的方程式________;此反应中碳元素的化合价如何变化:____。
(2) [查阅资料]纳米铁粉在空气中会自燃。
“铁丝在空气中很难燃烧,纳米铁粉却可以在空气中自燃”,你对燃烧的条件有了哪些新的认识:________。