题目内容
用氢氧化钠固体配制一定质量分数的氢氧化钠溶液,需要的实验步骤是
- A.溶解、过滤、蒸发
- B.溶解、称量、计算
- C.称量、溶解、计算
- D.计算、称量、溶解
D
分析:配制一定溶质质量分数的溶液,正确操作步骤为:计算、称量、溶解,可以据此解答该题.
解答:配制一定质量分数的食盐溶液,操作方法为:
1、计算所需氢氧化钠和水的质量.
2、用托盘天平称量所需氢氧化钠的质量,倒入烧杯中.
3、用量筒量取所需的水,倒入盛有氢氧化钠的烧杯中,用玻璃棒搅拌使其溶解.
故配制一定质量分数的氢氧化钠溶液,主要实验步骤依次是:计算,称量,溶解
故选D.
点评:很多实验题目都是从课本中的实验演变而来的,所以同学要熟练掌握课本中涉及到的典型试验,这样无论从哪个方向出的题目,同学们都能应付.
分析:配制一定溶质质量分数的溶液,正确操作步骤为:计算、称量、溶解,可以据此解答该题.
解答:配制一定质量分数的食盐溶液,操作方法为:
1、计算所需氢氧化钠和水的质量.
2、用托盘天平称量所需氢氧化钠的质量,倒入烧杯中.
3、用量筒量取所需的水,倒入盛有氢氧化钠的烧杯中,用玻璃棒搅拌使其溶解.
故配制一定质量分数的氢氧化钠溶液,主要实验步骤依次是:计算,称量,溶解
故选D.
点评:很多实验题目都是从课本中的实验演变而来的,所以同学要熟练掌握课本中涉及到的典型试验,这样无论从哪个方向出的题目,同学们都能应付.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
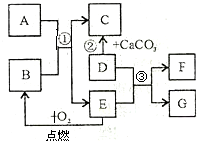 初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题:
初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题: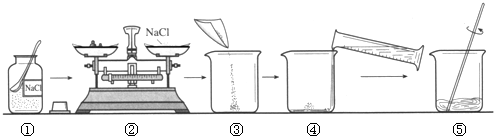
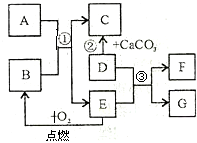 初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题:
初中化学常见物质A-G有如右图所示的转化关系(部分反应条件及物质已略去),已知A、C所含元素相同且均为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位;F是最轻的气体.请回答下列问题: