题目内容
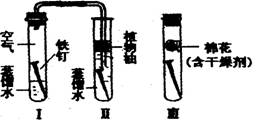
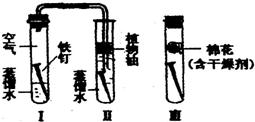 19、在探究铁生锈的实验中,为了证明铁生锈有氧气参与反应,小明改进了教材的装置(导管中有水)如下,试回答:
19、在探究铁生锈的实验中,为了证明铁生锈有氧气参与反应,小明改进了教材的装置(导管中有水)如下,试回答:(1)这种改进的优点是
证明铁生锈确实有氧气参加
;(2)你认为实验Ⅲ中的干燥剂可能是
氯化钙(或固体氢氧化钠)
;(3)实验前,处理久置的蒸馏水时进行加热煮沸这种除去水中氧气的原理是
温度升高,氧气的溶解度减小
;在给铁钉除锈时,小明将带锈的铁钉放人稀盐酸中进行加热,发现不易除去铁锈原因是
加热盐酸时挥发出氯化氢,盐酸的酸性降低
;(4)数天之后,为什么试管Ⅱ中的水进入试管I中,原因是
铁钉生锈消耗氧气,使I试管内压强减小,II试管内的水被吸入I试管
.分析:(1)隔绝了空气,更能够得出生锈的条件;
(2)能作为干燥剂的固体有氯化钙和氢氧化钠等;
(3)气体的溶解度随温度的升高而降低;盐酸是氯化氢的水溶液,所以温度升高会使氯化氢挥发出来;
(4)根据气体的压强来解答该题.
(2)能作为干燥剂的固体有氯化钙和氢氧化钠等;
(3)气体的溶解度随温度的升高而降低;盐酸是氯化氢的水溶液,所以温度升高会使氯化氢挥发出来;
(4)根据气体的压强来解答该题.
解答:解:(1)隔绝了空气能够更充分的得出铁生锈确实与氧气有关;
(2)能够作为干燥解答固体常见的为氯化钙和氢氧化钠;
(3)气体的溶解度随温度的升高而降低;盐酸是氯化氢的水溶液,所以温度升高会使氯化氢挥发出来,而使盐酸的酸性降低;
(4)铁钉生锈要消耗氧气,由于氧气的减少而使I试管内压强减小,II试管内的水被吸入I试管;
故答案为:
(1)证明铁生锈确实有氧气参加;
(2)氯化钙(或固体氢氧化钠);
(3)温度升高,氧气的溶解度减小;加热盐酸时挥发出氯化氢,盐酸的酸性降低;
(4)铁钉生锈消耗氧气,使I试管内压强减小,II试管内的水被吸入I试管.
(2)能够作为干燥解答固体常见的为氯化钙和氢氧化钠;
(3)气体的溶解度随温度的升高而降低;盐酸是氯化氢的水溶液,所以温度升高会使氯化氢挥发出来,而使盐酸的酸性降低;
(4)铁钉生锈要消耗氧气,由于氧气的减少而使I试管内压强减小,II试管内的水被吸入I试管;
故答案为:
(1)证明铁生锈确实有氧气参加;
(2)氯化钙(或固体氢氧化钠);
(3)温度升高,氧气的溶解度减小;加热盐酸时挥发出氯化氢,盐酸的酸性降低;
(4)铁钉生锈消耗氧气,使I试管内压强减小,II试管内的水被吸入I试管.
点评:解答本题要充分理解铁生锈的条件方面的知识,只有这样才能找出防止铁生锈的方法.

练习册系列答案
相关题目